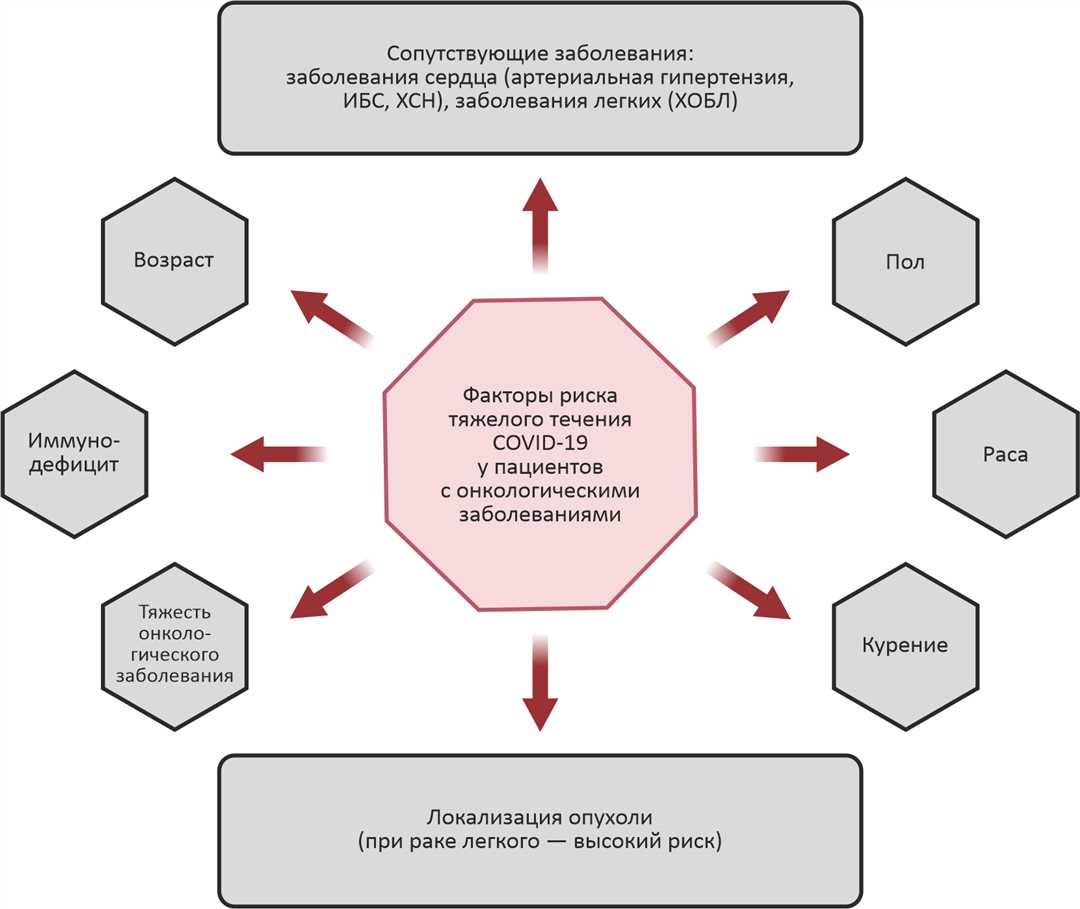
В начале 2020 года по всему миру началась эпидемия COVID-19, вызванная SARS-CoV-2 — одним из coronavirus, ассоциируемых с тяжёлыми респираторными заболеваниями. С тех пор исследования ученых толкают нас к более глубокому пониманию молекулярных механизмов, лежащих в основе этой инфекции и развивающейся к ней иммунной системы.
Coronaviruses обнаруживаются не только в легких, но и в мозге, где они способны вызвать neuroinvasive pathol. Механизмы регуляции микроциркуляторного тонуса и поствакцинальных реакций на внутрисосудистое воздействия вируса — темы, вызывающие больше интереса у исследователей.
В последние годы молекулярная биология стала незаменимым инструментом для понимания различных болезней. С помощью масс-спектрометрией и других омиксных технологий исследователи выявляют аберрантных рецепторы, которые играют важную роль в развитии COVID-19 и других связанных с ней diseases, такими как пневмония и миелина в нервной системе. Молекулярная разработка antiviral drugs, специфических для SARS-CoV-2, может повысить эффективность лечения и снизить риски для пациентов.
Одна из ключевых особенностей этого вируса — его способность инфицировать клетки с высокой скоростью и вызывать гибель клеток через механизмы апоптоза и разрушение клинической функции. Поэтому, важной компонентой исследований является разработка новых вакцин, которые могут эффективно усилить иммунную защиту организма и предотвратить развитие тяжелых форм заболевания.
Роль шиповых белков в проникновении в клетку
Исследователи обнаружили, что шиповые белки имеют высокую аффинность к рецепторам, присутствующим на поверхности клетки. В настоящее время известно, что таким рецептором для SARS-CoV-2 служит ангиотензин-конвертирующий фермент II (ACE2), который экспрессируется в различных тироцитах, эндотелиоцитах и других клетках различных тканей.
Взаимодействие между шиповыми белками вируса и рецептором ACE2 на поверхности клетки играет ключевую роль в проникновении SARS-CoV-2 в организм. При этом происходит активная эндоцитоз вирусной частицы, в результате чего он внедряется в клетку, нанося повреждение и нарушая молекулярную целостность.
В процессе попадания в клетку возникают множество биологических реакций, которые в итоге приводят к активации иммунной системы, освобождению воспалительных медиаторов и развитию патогенности. Известно, что шиповые белки SARS-CoV-2 способны вызвать повреждающее воздействие на эндотелиальные клетки, вызывая гибель их функций и повреждение сосудистой стенки.
Шиповые белки также играют роль в активации иммунной системы и индукции воспалительных цитокинов. В результате вирусного нападения происходит активация сигнального пути NF-κB, что вызывает повышенное выделение цитокинов, таких как интерлейкин-1β (IL-1β) и интерлейкин-6 (IL-6), а также фактор некроза опухоли α (TNF-α). Это может привести к развитию цитокинового шторма, который является одним из связанных с COVID-19 осложнений.
Роль шиповых белков SARS-CoV-2 в проникновении в клетку и патогенезе COVID-19 все еще находится в процессе исследования. Однако, результаты исследований говорят о том, насколько важными являются эти молекулы для реализации вирусного инфицирования и размножения. Они могут быть потенциальной мишенью для разработки новых противовирусных терапий и вакцин.
Влияние омиксных технологий на понимание молекулярных механизмов патогенности SARS-CoV-2 и SARS-CoV
Обнаружив в молекулярной ткани различные факторы, ответственные за развитие симптомов и тяжести инфекции, исследователи смогли лучше понять молекулярные механизмы патогенности SARS-CoV-2 и SARS-CoV. В последнее время значительный прогресс в этой области был достигнут благодаря использованию омиксных технологий, которые позволяют анализировать множество генов, белков и других молекул одновременно.
Одной из основных проблем при изучении коронавирусов является их повышенная степень аутореактивности, которая может привести к различным патологическим реакциям в организме. Исследования показали, что SARS-CoV-2 взаимодействует с белками-мишенями в микроциркуляции и активизирует воспалительные реакции со стороны иммунной системы. Такое взаимодействие может приводить к повреждениям сосудистой системы и повышению уровня воспалительной ответа.
Помимо того, что SARS-CoV-2 обладает способностью взаимодействовать с клетками хозяина, этот вирус также имеет способность активизировать белки-мишени, связанные с различными патологическими процессами. Особое внимание уделяется белку салмина как молекулярному механизму патогенности SARS-CoV-2 и SARS-CoV.
Омиксные технологии позволяют изучать представителей коронавирусной инфекции, а также другие болезни, вызванные коронавирусами, на более высоком уровне, позволяя нам лучше понять молекулярные механизмы развития этих болезней. Они также помогают в оценке возможных способов борьбы с инфекцией и разработке новых лекарственных препаратов.
С другой стороны, омиксные технологии также увеличивают нашу глубину понимания патогенных механизмов и происхождения SARS-CoV-2 и SARS-CoV. Они позволяют нам исследовать различные биологические и химические процессы, включая взаимодействия между вирусом и хозяйским организмом, а также реакции на уровне клетки и ткани.
Также стоит отметить, что омиксные технологии имеют значительное влияние на клиническую практику и пост-covid состояние пациентов. Они позволяют нам изучать молекулярные механизмы различных болезней, вызванных коронавирусами, такие как утомляемость, повреждения легких и повышенный уровень норадреналина. Это позволяет нам разрабатывать новые подходы к диагностике и лечению этих болезней.
В целом, использование омиксных технологий открывает новые перспективы в изучении молекулярных механизмов патогенности SARS-CoV-2 и SARS-CoV. Они позволяют нам более глубоко понять причины развития болезней и идентифицировать потенциальные мишени для лечения и профилактики. На сегодняшний день такие технологии активно внедряются и развиваются в России, и внедрение омиксных технологий в клиническую практику может значительно повысить эффективность диагностики и лечения коронавирусных инфекций.
Функция гликопротеина «Шип»
Один из важных молекулярных механизмов, вовлеченных в этот процесс, связан с участием металлопротеиназ. Исследования показали, что гликопротеин «Шип» взаимодействует с металлопротеиназами, что способствует разрушению клеточных структур и облегчает проникновение вируса внутрь клетки.
Функция гликопротеина «Шип» включает его способность связываться с рецепторами на клеточной мембране, что позволяет вирусу проникать в различные типы клеток. Проникновение коронавируса в клетку обеспечивается механизмом слияния вирусной оболочки с клеточной мембраной и образованием пузырей, внутри которых вирус попадает в клеточный цитоплазму.
Гликопротеин «Шип» также играет важную роль в размножении вируса внутри клетки. Он участвует в процессе сборки новых вирусных частиц, образуя специфические структуры, которые служат матрицей для сборки генетического материала внутри вирусных частиц.
Кроме того, гликопротеин «Шип» выполняет важную функцию в патогенезе коронавирусной инфекции. Он является мишенью для антител и иммунных клеток организма, что активирует иммунную систему и способствует нейтрализации и уничтожению вируса. Однако, этот процесс может иметь и негативные последствия, так как слишком высокий уровень антител может привести к развитию аутоиммунного процесса и аберрантных иммунных реакций.
Исследования гликопротеина «Шип» и его функции в развитии коронавирусной инфекции позволяют лучше понять молекулярные механизмы патогенеза этого заболевания. Они также способствуют разработке новых методов профилактики и лечения вирусных инфекций, включая новые штаммы коронавируса.
Взаимодействие с мембранами клетки
Основная роль ангиотензин-конвертирующего фермента заключается в превращении ангиотензина I в ангиотензин II, действие которого способствует сужению сосудов, свертыванию крови и повышает кровяное давление. Некоторые исследования указывают на возможность использования ангиотензина-1-7 в качестве потенциального лекарственного средства для дальнейшего развития вакцин и препаратов для лечения коронавирусной инфекции.
Другим ключевым элементом взаимодействия между вирусом и клеткой являются рецепторы. Они могут быть использованы в качестве мишеней для разработки вакцин и лекарственных препаратов, которые вызывают иммунный ответ организма и предотвращают проникновение вируса в клетки.
Исследования показывают, что SARS-CoV-2 способен вызывать повреждения микроциркуляции и разрушать легочную ткань. Это может повышать риск развития патологических процессов и осложнений пост-COVID состояний, таких как пост-ковидный синдром и невроинвазия. Взаимодействие вируса с клеточными мембранами может провоцировать воспалительные процессы и активировать иммунную систему, вызывая иммунный ответ организма в виде высвобождения цитокинов, таких как IL-12, и активации T-хелперов, стимулирующих иммунные отклики.
Также было выявлено взаимодействие между вирусом и циклофилином, что может иметь значение для дальнейшей реализации новых технологий и разработки веществ, направленных на подавление размножения вируса и предотвращение его повреждающего действия на клетки и органы.
Процесс репликации вируса внутри клетки
Коронавирусы, включая вирус SARS-CoV-2, который вызывает заболевание COVID-19, инфицируют респираторный эпителий верхних дыхательных путей. Их внедрение в клетки эпителия осуществляется через присутствующую на вирусе оболочку и структуру, называемую «шипами», которые взаимодействуют с рецепторами клетки. Вследствие этого вирус попадает внутрь клетки и начинает репликацию.
Процесс репликации вируса поддерживается биологическими механизмами внутри клетки. Вирус использует иммунный ответ клетки для своего размножения. Важную роль в этом процессе играют белки-мишени клетки — IL-35, TNF-α и норадреналин, которые активизируются в результате взаимодействия с вирусом. Эти белки запускают иммунные реакции, которые стимулируют развитие внутрисосудистого воспаления и изменения в работе эпителия.
Как показывают исследования, вирус вызывает различие в патогенезе COVID-19. В легком случае заболевания он активизирует иммунные реакции и способствует быстрому разрешению воспаления. Тем не менее, в некоторых случаях вирус проникает в эпителиальные клетки микрососудов, что приводит к развитию внутрисосудистого воспаления, образованию тромбов и осложнениям, связанным с повреждением мозга.
Используя масс-спектрометрию, авторы исследования выявили, что при инфицировании коронавирусами происходят изменения в составе белков-мишеней клетки, а также нарушения в работе клеточных рецепторов. Эти изменения способствуют размножению вируса и приводят к проявлениям заболевания COVID-19.
Острый иммунный ответ на вирус может вызывать нервную утомляемость и различные проявления нервных осложнений. Также известно, что цитокин TNF-α может вызывать воспалительные изменения в мозге, что может быть связано с нейрологическими симптомами COVID-19.
Амбигуитетный характер репликации коронавирусов и их размножение в эпителии верхних дыхательных путей являются ключевыми факторами в патогенезе COVID-19. Понимание этих механизмов открывает новые перспективы для разработки вакцин и лекарств, нацеленных на предотвращение проникновения вируса в клетки и его размножения.
Влияние генетического материала на развитие инфекции
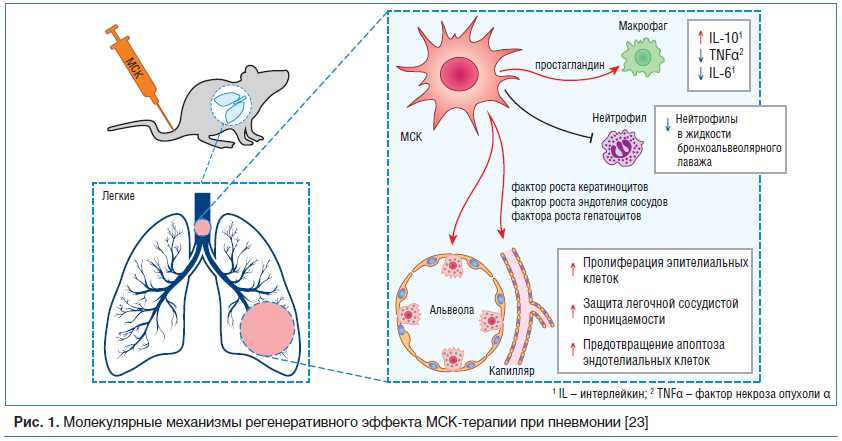
Генетическое материало коронавируса имеет крайне важное значение для развития инфекции у органов человека. Исследования, проведенные с использованием масс-спектрометрией и другими методами, позволили выявить влияние генетического материала на различные аспекты инфекции, такие как пост-covid синдром, риски развития болезней и снижение уровней противовирусного ответа.
Генетический материал коронавируса может взаимодействовать с различными рецепторами организма, активируя разные патологические процессы. Например, эндотельные клетки, которые являются мишенью вируса, подвергаются поражению и активации при взаимодействии с генетическим материалом вируса. Это явление называется «эндотелиальной мимикрией».
Исследования показали, что генетический материал коронавируса может приводить к поражению легочной эпителии и кровеносных сосудов, вызывая экссудативные явления и повреждение микроциркуляторного русла. Также выделены определенные эпитопы генетического материала, с которыми взаимодействуют различные иммунные клетки, такие как Т-лимфоциты и цитокины IL-7 и IL-35.
| Референсы: |
|
Возможные пути борьбы с коронавирусом на молекулярном уровне
На молекулярном уровне, возможные пути борьбы с коронавирусом включают использование технологий ингибирования взаимодействия между «шипами» вируса и рецепторами клетки-хозяина. Одним из известных способов торможения этого взаимодействия является использование антител, которые образуются в иммунной системе человека после заражения SARS-CoV-2 либо через вакцинацию. Эти антитела могут связываться с «шипами» и мешать их взаимодействию с рецепторами клеток, что приводит к снижению инфекционного процесса и тяжести болезни.
Новым подходом к борьбе с коронавирусом на молекулярном уровне является использование мимикрии – процесса, при котором используются молекулярные структуры, очень похожие на те, что присутствуют на поверхности вирусных «шипов». Это позволяет отвлечь внимание внимания вируса на себя и предотвратить его взаимодействие с клетками-мишенями. Валерий Лопатин и его коллеги предложили использовать этот подход в исследованиях с SARS-CoV-2 и другими патогенными вирусами.
Также, одним из возможных путей борьбы с коронавирусом на молекулярном уровне является активность некоторых молекулярных компонентов в организме, которые могут влиять на функцию клеток-мишеней. Например, исследования показывают, что активация специфической цитокиновой реакции и другими коммуникационными сигналами может усилить иммунные функции и защиту нервной системы и эндотелиев нашего организма.

0 Комментариев