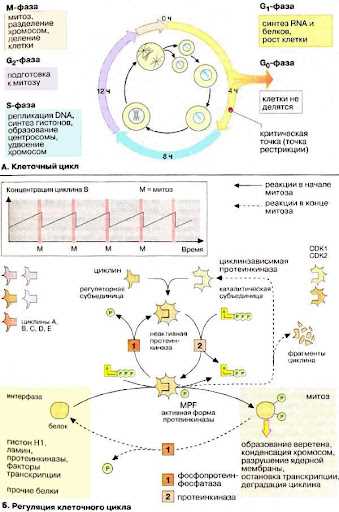
Клеточный цикл — это сложный и строго регулируемый процесс, который играет важную роль в жизни всех клеток. Он включает в себя несколько фаз: G1, S, G2 и M, каждая из которых характеризуется определенными молекулярными событиями и функциональными изменениями. S фаза, также называемая фазой синтеза, является ключевым этапом клеточного цикла, во время которого происходит репликация ДНК и подготовка к делению клетки.
Регуляция s фазы клеточного цикла осуществляется с помощью комплексных молекулярных механизмов, включающих участие ряда ключевых молекул и белков. Одним из главных участников этого процесса является группа белков, называемых циклин-зависимыми киназами (CDK), которые взаимодействуют с циклинами и активируются в определенные моменты времени. CDK играют важную роль в контроле прогресса клеточного цикла и являются своего рода пусковыми реакциями для различных этапов цикла.
Однако, регуляция s фазы не ограничивается только синтезом ДНК и подготовкой к делению. На самом деле, существуют различные альтернативные пути, включая активацию апоптозных факторов или ингибиторов клеточной пролиферации. CDK также участвуют в регуляции этих путей, что дает клетке возможность решить, продолжать ли репликацию ДНК или инициировать программированную клеточную смерть.
Понимание молекулярных механизмов регуляции s фазы клеточного цикла является ключевым для практических применений в медицине и различных областях науки. Это позволяет разрабатывать новые методы лечения рака и других заболеваний, связанных с нарушениями клеточного цикла. Более того, эти исследования могут расширить наше понимание эволюции и происхождения жизни, так как клеточный цикл и его регуляция важны для всех организмов, от бактерий до человека.
Вначале был митоз
Молекулярно-генетические методы представляют собой важный инструмент в исследованиях митоза. В начале цикла, происходит запуск событий, после которого клетка переходит в стадию деления, что поддерживается информационной системой.
Комплексы Cdk1/циклин: ключевые регуляторы митотической регуляции
Cdk1/циклин комплексы являются ключевыми регуляторами в процессах митоза. Эти комплексы состоят из постоянно синтезирующихся циклинзависимых киназ и регуляторных подединиц. Во время разных стадий митоза, разные циклины связываются с Cdk1 и активируют его, что позволяет клетке переходить от одной фазы к другой.
Кребсов цикл, комплексы протеолиза и их роль в регуляции митоза
Важную роль в регуляции митоза играют такие комплексы, как комплекс кребса и каспазы. Комплекс кребса осуществляет регуляцию межфазного контроля и гарантирует корректную передачу клеточного материала между покоящимся и делающимся состояниями. В свою очередь, каспазы, ферменты пролиферации, участвуют в процессе протеолиза и контролируют деструкцию клеточных структур во время цикла.
Семейство циклин-зависимых киназ: характеристика и роль в митозе
Циклин-зависимые киназы (ЦЗК) являются семейством регуляторов клеточного цикла, которые участвуют в митозе. Они контролируют разные стадии клеточного цикла и имеют различные функции. Например, Cdk1-циклин комплексы активируются в ранних стадиях митоза и выполняют функцию разбора хромосом, а Cdk2-циклин комплексы контролируют фазу С перед делением клеток.
В итоге, молекулярные механизмы регуляции s фазы клеточного цикла — сложная система, где многое зависит от взаимодействия комплексов и регуляторных белков. Исследования в этой области продолжаются, и поиск новых методов и подходов позволяет углубить наше понимание молекулярных событий, происходящих в митозе.
ДНК-репликация: начало событий
На первом этапе репликации активируются циклинзависимая киназа (ЦДК) и фосфорилирование образом, которые играют важную роль в контроле разного количества генов. ЦДК активируется путем связывания с циклинами, которые есть в разных группах и имеют названия А, В, Д и т.д. Отдельные циклины могут быть способны активировать разные ЦДК, что помогает в репликации ДНК, транскрипции генов и другим процессам в клетке.
Результаты исследований различных ученых и моделей говорят о том, что продолжительность S фазы может быть изменена в зависимости от разных факторов. Некоторые исследователи связывают продолжительность S фазы с активацией определенных транскрипционных факторов, которые способны поддерживать репликацию ДНК. Другие исследования указывают на роль ЦДК и циклинозависимых киназ в контроле времени, необходимого для репликации ДНК.
В процессе ДНК-репликации одним из ключевых событий является активация митотического цикла и контрольные точки, которые позволяют клеткам поддерживать нормальную репликацию ДНК и предотвращать некроз. Это достигается благодаря тесному взаимодействию между различными факторами и молекулами, такими как циклины, ЦДК и комплексы протеинов, ответственных за протеолиз.
Существуют разные модели и теории, объясняющие начало событий в ДНК-репликации. Одной из таких моделей является модель «печатного станка», которая предлагает взглянуть на репликацию ДНК как на сложный и динамичный процесс, который постепенно запускается и поддерживается на протяжении всего клеточного цикла.
Хартуэлл и его коллеги предложили другую модель, в которой активация репликации ДНК происходит в результате активации комплексов ЦДК и фосфорилирования различных факторов. Эти комплексы образуются под воздействием разных веществ, таких как циклины, и играют важную роль в регуляции репликации ДНК.
Таким образом, ДНК-репликация представляет собой сложный и утомительный процесс, включающий взаимодействие различных молекул и факторов в клетке. Начало событий в репликации ДНК связано с активацией различных циклинозависимых киназ и контрольных точек, которые играют важную роль в успешном прохождении клеточного цикла и поддержании нормальной пролиферации клеток.
Фосфорилирование и деградация Cdk

Фосфорилирование Cdk происходит в определенных местах и времени, исходя из требований клетки. Возможно, что фосфорилирование Cdk служит для проверки готовности клетки к переходу в следующую фазу цикла. Недавние исследования позволяют более глубоко проникнуть в молекулярные механизмы этого процесса.
Фосфорилирование Cdk обеспечивает активацию комплекса Cdk-циклин и его участие в клеточном делении. Во время фосфорилирования, определенные белки, такие как ингибиторы Cdk (Cip / Kip) и фосфатазы типа 1, играют важную роль в регуляции активности Cdk.
Деградация Cdk осуществляется с помощью протеасом, главным образом через убиквитин-зависимый путь. Во время фазы G1 и M, Cdk-циклин комплексы подвергаются убиквитинированию и последующей протеолизу. Этот процесс связан с молекулярными механизмами апоптоза и другими процессами, связанными с регуляцией клеточного цикла.
Ингибиторы Cdk (Cip / Kip) также играют важную роль в деградации Cdk, предотвращая образование активного комплекса Cdk-циклин и подавляя деление клеток. Вороны фосфорилирования и деградации Cdk и их взаимосвязи являются основными ключами для понимания регуляции клеточного цикла.
Роль циклин-зависимых киназ
Циклин-зависимые киназы (ЦЗК) играют ключевую роль в регуляции клеточного цикла и обеспечении правильного протекания с фазы клеточного цикла в другую. ЦЗК представлены семейством серин/треонинкиназ, среди которых наиболее хорошо изучены Cdk1 (циклин B-зависимая киназа) и Cdk4 (циклин D-зависимая киназа).
Циклины – это белки, которые образуют комплексы с ЦЗК и активируют их киназную активность. Циклины влияют на работу ЦЗК в зависимости от фазы клеточного цикла. Так, в начале s фазы клеточного цикла, активная комплексная форма cdk1 циклин активирует процессы ДНК-репликации. В пролиферационном процессе клетки при синтезе ДНК и делении клетки также активируется комплекс k1 циклин с циклином B. Вместе с циклинами существуют ингибиторы циклин-зависимых киназ, которые проверяют и устраняют ошибки в работе клетки.
Циклин-зависимые киназы и регуляция клеточного цикла
Циклин-зависимые киназы являются ключевыми регуляторами клеточного цикла. Они фосфорилируют множество молекулярных регуляторов клеточного цикла, которые в свою очередь контролируют переход клетки через различные фазы клеточного цикла. Регуляция с точки зрения циклических колебаний состоит из двух параллельных циклов и является взаимосогласованной между ними: образование комплексов ЦЗК-циклин усиливает их активность, тогда как фосфорилирование киназой активности y активации зависимая наличие фактора таких как ингибиторы циклин-зависимых киназ, которые поддерживают демпфер в процессе.
Существуют различные теории относительно роли циклин-зависимых киназ в клетках и в различных пролиферативных процессах. Сейчас исследователями изучается их взаимодействие с другими белками и молекулами, такими как сестринские киназы, регуляторы апоптоза и митохондриальной апоптозы, а также транскрипционные факторы.
Международные исследования в области циклин-зависимых киназ
Исследователи в области биологии клетки и молекулярной биологии сейчас активно изучают циклин-зависимые киназы и их роль в клеточном цикле и различных процессах клеточного деления. Одним из крупнейших достижений стало обнаружение в Saccharomyces cerevisiae (дрожжи) группы мутантов, которые не могли преодолеть суточные циклы клеточных делений, благодаря чему эти генетические мутанты называются циклическими.
Исследователи из Кребсовского института создали схему работы циклин-зависимых киназ и обнаружили концепцию взаимодействия с другими молекулами и белками, которая названа «циклинацикла». Также большое внимание уделяется разработке регуляторов активности циклин-зависимых киназ для использования их в лечении различных заболеваний, включая рак.
Таким образом, циклин-зависимые киназы играют важнейшую роль в регуляции клеточного цикла и поддержании его правильного протекания. Их взаимодействие с другими белками и молекулами влияет на выполнение различных процессов клеточного деления, таких как синтез ДНК и апоптоз.
Межфазный контроль и митогенные сигналы
Митогенные сигналы, также известные как сигналы роста, являются важным фактором активации циклин-зависимых киназ и, следовательно, циклов клеточного деления. Они активируют цитоплазматические рецепторы, что приводит к активации ферментов, таких как Ras, и активации циклин-зависимых киназ. Этот процесс помогает клетке пройти через «пусковые точки» и продолжить цикл деления.
Роль циклинам и митогенных сигналов в клеточном цикле и их взаимосвязь показана на схеме ниже:
Циклины: Циклины — это семейство белков, которые регулируют фазы клеточного цикла. Они вызывают активацию циклин-зависимых киназ и способны повышать их активность при связывании.
Митогенные сигналы: Митогенные сигналы — это сигналы роста, которые активируют циклин-зависимые киназы и помогают клетке пройти через «пусковые точки».
Видео «Молекулярные механизмы регуляции s фазы клеточного цикла» дает более подробное объяснение процесса функционирования цикла клеточного деления и роли циклин и митогенных сигналов:
Участие Р21-сигнального пути в регуляции клеточного цикла
Одна из ключевых цепей, способных проверять и контролировать процессы клеточного цикла, называется Р21-сигнальный путь. Этот путь играет важную роль в регуляции различных событий, которые происходят на протяжении всего клеточного цикла.
Р21-сигнальный путь включает в себя семейство белков, известных как циклины и циклинзависимые киназы (CDK). Они взаимодействуют с помощью циклинов и определенных ингибиторов, которые называются «секвестры». Это взаимодействие помогает активировать или ингибировать функцию комплексов CDK–циклин в разных фазах клеточного цикла.
С помощью микроаррей-анализа и других методов исследования удалось выяснить, что ключевые события, регулирующие клеточный цикл, такие как активация CDK–циклин комплексов и точка «печатного узла», контролируются сегментами генома, называемыми промоторами и энхансерами.
Кроме Р21-сигнального пути, в регуляции клеточного цикла участвуют такие семейства белков, как сестринские гены и семейство митохондриальных супероксиддисмутаз (SOD). Они играют важную роль в процессах пролиферации и регулировании межклеточного сигнала.
Ферменты, а также комплексы CDK1–циклин, активируются в различных фазах цикла и взаимодействуют с другими факторами, помогая клетке готовиться к делению. Семейство циклинов, включая циклин D, циклин E и другие, активируются в зависимости от фазы клеточного цикла и играют ключевую роль в активации CDK–циклин комплексов.

0 Комментариев