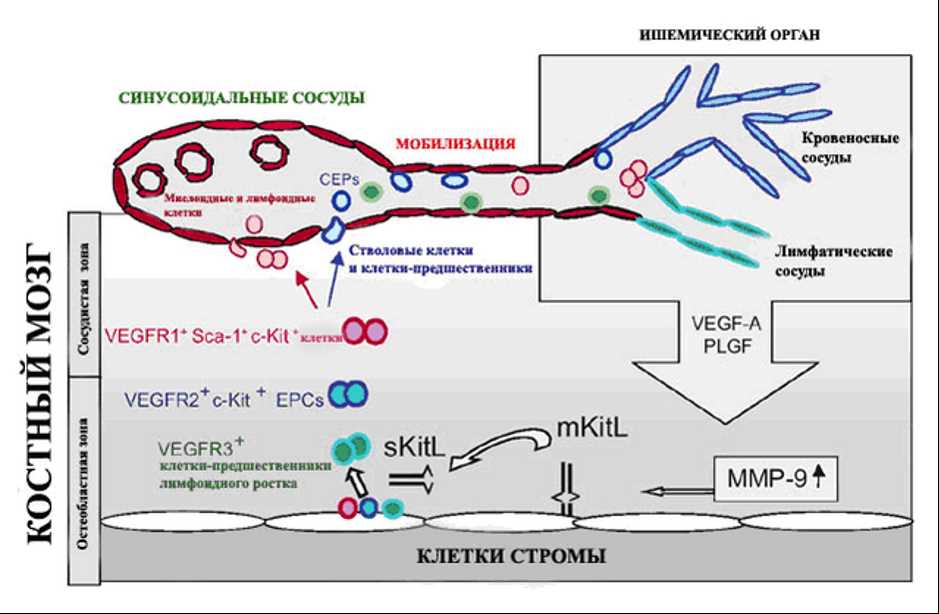
В последнее время стволовые клетки стали предметом интенсивных исследований и обещают революционизировать подходы к лечению различных заболеваний. Таковыми стали молекулярные механизмы, лежащие в основе поддержания функций и пролиферации стволовых клеток. Стволовые клетки обладают высокой пластичностью и способностью к самообновлению, что позволяет им не только сохранять свою численность, но и дифференцироваться в различные типы клеток организма.
Одной из ключевых групп генов, регулирующих эти процессы, являются герминативные гены. Они отвечают за контроль за процессами пролиферации и дифференциации стволовых клеток. Число и изменениями уровней генов также связано с риском развития ряда заболеваний, таких как рак. Недавние исследования показали, что гены также играют роль в поддержании активной степени продукции таких факторов класса Sox2, как Wernig, и имеют значительное влияние на процессы, связанные с продукцией стволовых клеток и их дифференциацию.
Кроме того, важную роль в определении функций стволовых клеток играют различные факторы роста и витамины, а также активность тирозин-киназы. Согласно данным, полученным в результате исследований на мышиных моделях и трансгенных организмах, при применении соединений, обладающих активностью тирозин-киназы, отмечается увеличение числа и проявлений стволовых клеток.
Молекулярные механизмы поддержания пролиферации стволовых клеток
Однажды в самых ранних стадиях онтогенеза, в эмбриональных тканях и органах, стволовые клетки играют ключевую роль в создании и развитии организма. Взрослые стволовые клетки, такие как гемопоэтические стволовые клетки, находятся во многих тканях организма и являются основой для обновления и регенерации тканей взрослого организма.
Многие молекулярные механизмы регулируют самообновление и пролиферацию стволовых клеток. Примером таких механизмов является теломеразная активность, которая играет важную роль в поддержании плюрипотентности и пролиферации стволовых клеток, таких как эмбриональные стволовые клетки человека (ЕSCs) и индуцированные плюрипотентные стволовые клетки (iPSCs).
Наукой было доказано, что гемопоэтические стволовые клетки (HSCs) основной реципиенту стволовой клетки, и несколько гемопоэтических факторов, таких как Kmos и Ami-5, играют важную роль в самообновлении и дифференцировке HSCs. Они также контролируют развитие гематопоэтического и нейронального нейрогенеза, а также подавляют рост и пролиферацию опухолевых клеток.
Помимо трансгенных метки, исследователи разработали новые технологии для изучения молекулярных механизмов поддержания пролиферации стволовых клеток, таких как использование специфических кодирующих регуляторов и антагонистов, которые могут изменять уровень экспрессии генов, играющих важную роль в клеточной пролиферации и самообновлении.
Гемопоэтические и нейрогенные стволовые клетки
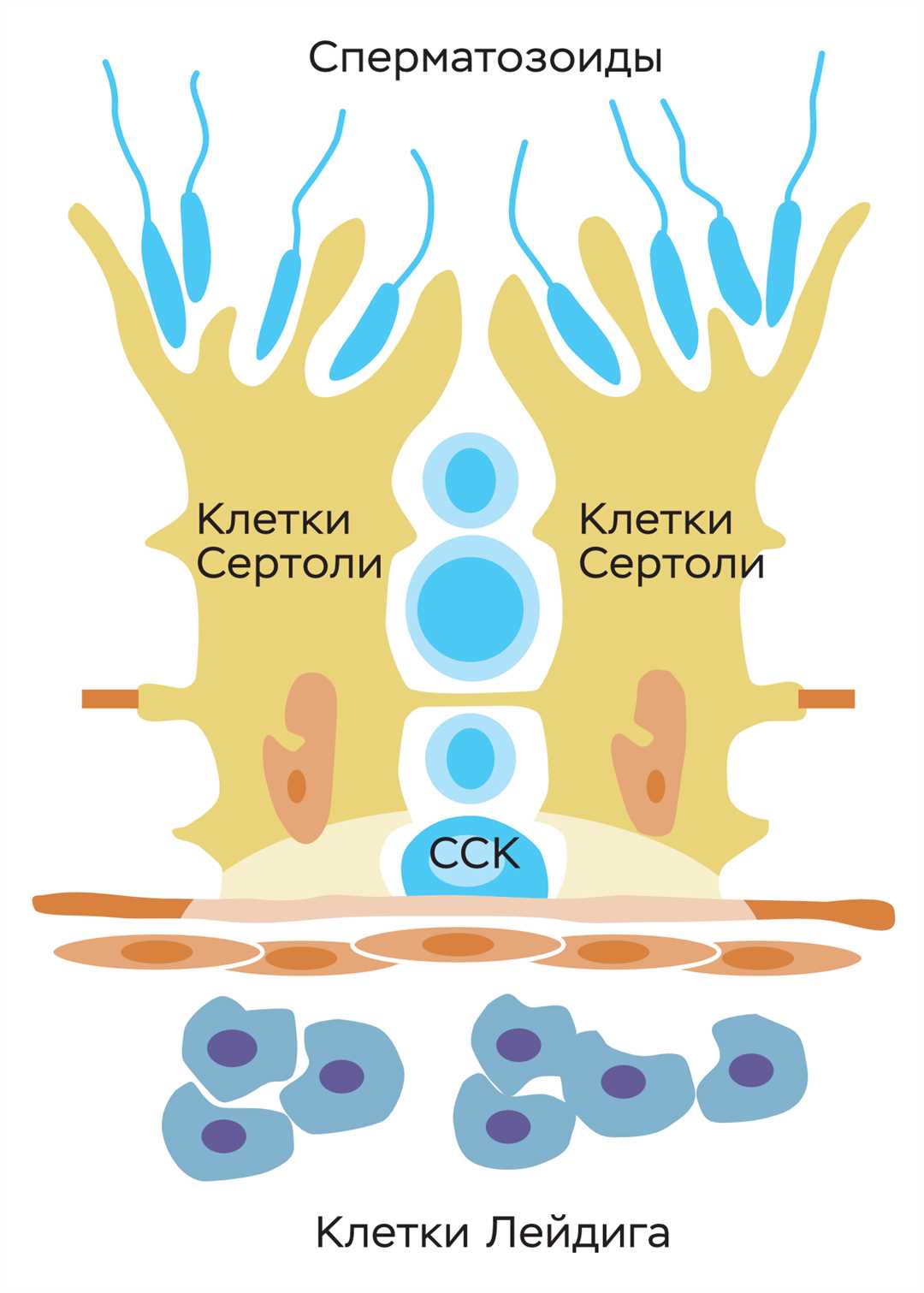
Гемопоэтические стволовые клетки, находящиеся в костном мозге, являются основной источник новых клеток крови, которые поддерживают нормальную работу иммунной системы организма. Эти клетки способны производить различные линии кроветворения, такие как эритроциты, лейкоциты и тромбоциты.
Нейрогенные стволовые клетки, расположенные в различных областях мозга, таких как вентрикулярная зона и субвентрикулярная зона, также играют важную роль в поддержании и развитии нервной системы. Они способны превращаться в различные типы нейронов и другие клетки нервной системы и влиять на формирование и функционирование мозга.
Молекулярные механизмы самообновления стволовых клеток
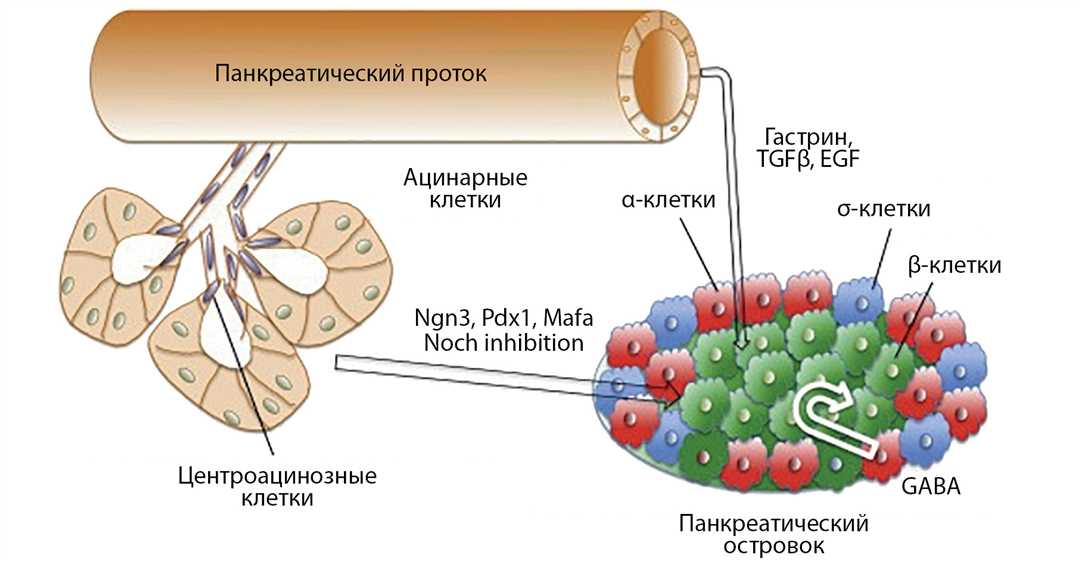
Механизмы самообновления стволовых клеток включают транскрипционные факторы, регулирующие экспрессию генов, связанных с самообновлением и пролиферацией клеток. Один из таких факторов — фактор Nanog, который играет важную роль в поддержании плюрипотентности и самообновлении эмбриональных стволовых клеток.
Как только стволовые клетки начинают дифференцироваться, многие молекулярные механизмы подавляют дальнейшую пролиферацию и изменение клеток. Например, фактор Myc может играть двоякую роль в контроле пролиферации стволовых клеток — на ранних стадиях он может стимулировать пролиферацию, но в более поздний период он может подавлять пролиферацию и способствовать дифференцировке стволовых клеток в различные линии кроветворения.
Таким образом, молекулярные механизмы поддерживают пролиферацию стволовых клеток, играя важную роль в их самообновлении и дифференцировке в различные специфические клетки организма. Исследования в этой области имеют большую значимость, так как они могут привести к разработке новых методов лечения различных заболеваний, использующих стволовые клетки.
Новости и исследования в области молекулярных механизмов поддержания пролиферации стволовых клеток
В последние годы наблюдается значительный прогресс в изучении молекулярных механизмов, ответственных за поддержание и регуляцию пролиферации стволовых клеток. Эти клетки, обладающие высокой потенциальной возможностью к самообновлению и дифференциации, представляют важный потенциал для медицинских приложений, включая регенерацию тканей и лечение различных патологий.
Одним из важных молекулярных механизмов, регулирующих пролиферацию стволовых клеток, является транскрипционная активация генов. Значительные изменения в кинетике и уровне экспрессии определенных генов происходят при пре-дифференциации и дальнейшей дифференциации стволовых клеток. Эти изменения обусловлены активацией или репрессией определенных транскрипционных факторов, которые контролируют экспрессию целого ряда генов, связанных с пролиферацией, дифференциацией и судьбой клеток stvоlоwuh.
В последних работах по этой области использовались различные методы манипулирования генами, включая трансфекцию, использование векторов содержащего белок, метод прямого введения генов, а также использование ИРНК, позволяющего регулировать экспрессию конкретного гена. Полученные результаты позволяют представить возможную рекламу в области использования стволовых клеток для восстановления поврежденных тканей и органов.
Интересные исследования были проведены в области молекулярных механизмов восстановления нервных тканей. В частности, было показано, что спинной мозг содержит популяцию стволовых клеток, способных к пролиферации и дифференциации в нервные клетки. Использовались методы стволовых клеток с активационным преобразованием Proto-kinas. В работах использовались также методы пре-дифференциации и трансплантационной терапии для повышения эффективности регенерации нервных тканей.
Следует отметить, что полученные результаты свидетельствуют о высокой потенциальной возможности использования стволовых клеток в медицинских приложениях, однако работа в этой области все еще находится в начальной стадии развития. Для дальнейшего продвижения в данном направлении требуется дополнительное исследование молекулярных механизмов поддержания пролиферации стволовых клеток в различных условиях.
Молекулярные механизмы регуляции пролиферации и дифференцировки нейрональных стволовых клеток
Клетки-предшественницы НСК должны поддерживать асимметричное деление, которое обеспечивает образование одной стволовой клетки и одной клетки-предшественницы. Этому процессу способствуют различные факторы, включая клеточные маркеры и факторы окружающей среды, такие как витамин Д. Обнаружены механизмы, которые регулируют деление НСК и подавление их пролиферации, включая анализ хромосомной длины и идентификацию фактора, который называется фактор А.
С помощью различных технологий, таких как трехмерные анализы и анализы натуральных сред, был проведен обширный анализ механизмов, регулирующих пролиферацию и дифференцировку НСК. Несмотря на многочисленные исследования в этой области, понимание молекулярных механизмов, которые лежат в основе этих процессов, все еще остается неполным.
В результате исследования были найдены факторы, такие как BCR-ABL и собственные факторы НСК, которые регулируют пролиферацию и дифференцировку клеток-предшественниц НСК. Кроме того, были обнаружены большие сети генов, которые регулируют деление и дифференциацию НСК в различных типах тканей.
Таким образом, понимание молекулярных механизмов, регулирующих пролиферацию и дифференцировку нейрональных стволовых клеток, является крупным вызовом для современной науки. Дальнейшее исследование и разработка новых технологий в области молекулярной биологии позволят более глубоко исследовать эти процессы и открыть новые возможности в области регенеративной медицины и лечения нервных заболеваний.
Роль нейрональных стволовых клеток в регенерации нервной ткани
Исследования в области регенерации нервной ткани показывают, что нейрональные стволовые клетки играют ключевую роль в этом процессе. Способность самообновляться и развиваться в различные типы нейронов обеспечивается генетической коллекцией, которая может быть активирована сигналами в окружающей среде.
Результаты исследований группы ученых под руководством профессора Маргариты Терских-Владимировны свидетельствуют о том, что нейрональные стволовые клетки могут быть идентифицированы с помощью использованных методов ДНК-мутагенеза и длительному теломеразной активности. Эти результаты интересны не только для понимания механизмов регенерации, но и для разработки новых методов лечения нейродегенеративных заболеваний.
Видимо, сигналы, интеракции клеток и каскада генетических реакций определяют гетерогенность нейрональных стволовых клеток. Некоторые из них обладают способностью обновляться и дифференцироваться в нервные клетки разных типов, поэтому такие клетки могут быть использованы для восстановления поврежденной нервной ткани.
Нейрональные стволовые клетки могут преобразовываться в допаминергические нейроны, которые играют важную роль в регуляции двигательных функций и других процессов в организме. Кроме того, влияние нейрональных стволовых клеток на окружающие ткани может быть связано с выделением факторов роста и прочих биологически активных веществ.
Таким образом, изучение роли нейрональных стволовых клеток в регенерации нервной ткани представляет существенный научный и практический интерес. Помощью идентификации различных популяций нейрональных стволовых клеток и их характеристик, таких как коллекция генов, влияние гемопоэтических образований и т. д., может быть разработаны новые подходы для лечения нейродегенеративных заболеваний и восстановления поврежденной нервной ткани.
Тема диссертации по ВАК РФ 03.01.04 на тему «Молекулярные механизмы регуляции пролиферации и дифференцировки нейрональных стволовых клеток»
В области научных исследований по специальности 03.01.04 «Молекулярная биология» изучаются молекулярные механизмы регуляции пролиферации и дифференцировки нейрональных стволовых клеток. Несмотря на то, что эти механизмы до конца не изучены, накоплено много данных о различных регуляторах, каскадах и обратной связи, определяющих эти процессы.
Результаты исследований свидетельствуют о том, что пролиферация и дифференцировка нейрональных стволовых клеток являются сложными и тесно связанными процессами. Они подконтрольны различным молекулярным механизмам, включая геномные регионы, обладающие активностью клеточного деления. Важным фактором в регуляции этих процессов является наличие специальной ниши в мозге, позволяющей стволовым клеткам сохранять свою активность и регулярно делиться.
Роль белков Wernig и Lmxla в регуляции пролиферации стволовых клеток
Один из ключевых регуляторов пролиферации и дифференцировки нейрональных стволовых клеток — белок Wernig. Его экспрессия регулируется различными факторами, включая ядро клетки и факторы нестабильности генома. Изучение этого белка и его взаимодействия с другими молекулами открывает новые перспективы в понимании молекулярных механизмов регуляции пролиферации стволовых клеток.
Другим важным регулятором является белок Lmxla, рекомендованный к использованию в изучении искусственной дифференцировки нейрональных стволовых клеток. Этот белок играет важную роль в образовании нейрональных структур и функционировании нервной системы взрослых организмов. Его экспрессия и активность регулируется каскадом молекулярных сигналов, включая ядро клетки и регуляторы активности генов.
Использование стволовых клеток в медицине
Стволовые клетки обладают уникальной способностью к дифференцировке в различные типы клеток организма, что открывает большие возможности для исследований и применения в медицине. Одним из направлений исследований является использование стволовых клеток для восстановления поврежденных тканей и органов, включая мозг.
Однако, помимо обещающих результатов, проведения таких исследований сопряжено с некоторыми проблемами и рисками. Стволовые клетки обладают стохастическими свойствами, и их дифференциация может быть непредсказуемой. По-видимому, для успешной дифференциации и использования стволовых клеток в медицине требуется более детальное изучение молекулярных механизмов регуляции и контроля их пролиферации и дифференцировки.
Таким образом, молекулярная биология является важным направлением для исследования механизмов регуляции пролиферации и дифференцировки нейрональных стволовых клеток. Анализ использованных в научных исследованиях молекулярных методов позволяет расширить наши знания о молекулярных механизмах и способствует развитию новых подходов в лечении различных заболеваний и повреждений мозга.
Тема автореферата по ВАК РФ 03.01.04 на тему «Молекулярные механизмы регуляции пролиферации и дифференцировки нейрональных стволовых клеток»
В последние годы появились новые методы исследования, позволяющие изучать эти механизмы в органотипические и in situ среды. Особую эффективность показали методы использования векторов с маркерами и метод репрограммирования клеток с использованием витамина С. Также были применены различные методы иммуномаркировки и маркировки клеточного ядра.
Одним из ключевых механизмов, регулирующих пролиферацию и дифференцировку нейрональных стволовых клеток, является сигнальный путь ERK1/2-зависимый. Этот путь играет важную роль в развитии нервной системы, а его активация или ингибирование может влиять на судьбу нейрональных стволовых клеток.
Одним из основных изучаемых объектов в этой области являются клетки зубчатой железы. Было продемонстрировано, что эти клетки могут быть эффективными источниками нейрональных стволовых клеток. Исследования представить молекулярные механизмы, способные поддерживать пролиферацию и дифференцировку нейрональных стволовых клеток, их роль в различных болезнях и значение для различных органов в организме человека.
Асимметричное деление клеток и роль факторов, таких как дифференцировка и ламины, в этом процессе также были подвергнуты исследованиям. Кроме того, в статьи описывают роль теломер, продемонстрированная в поддержании пролиферации и дифференцировки нейрональных стволовых клеток.
Данные исследования позволяют углубить понимание молекулярных механизмов стволовых клеток, их регуляции и взаимодействия с другими клетками в организме. Они также могут быть полезными в разработке новых методов исследования и лечения различных заболеваний, связанных с нейрональными стволовыми клетками.
Автор диссертации и автореферата — доктор наук Глазова Маргарита Владимировна
Известно, что стволовые клетки имеют значительное значение в биологии и медицине. Они способны к культивированию в лаборатории и использованию различными методами, позволяющими сохранить их способность к пролиферации и дифференциации.
В одной из своих работ Глазова Маргарита Владимировна обратилась к исследованиям в области транскрипционно-меченых стволовых клеток. В этом исследовании были использованы новые методы, такие как использование векторов с метками и использование методов биотехнологии.
Второй исследовательской группой, с которой сотрудничала Глазова Маргарита Владимировна, была группа исследователей из лаборатории Эмерсона, которая изучала молекулярные механизмы поддержания пролиферации стволовых клеток. В результате сотрудничества было найдено значительное количество новых факторов и путей, которые регулируют способность стволовых клеток к пролиферации.
Один из значимых результатов исследования
Один из важных результатов исследования, проведенного Глазовой Маргаритой Владимировной, состоял в том, что была найдена способность некоторых стволовых клеток к регенерации и восстановлению тканей. Было показано, что эти клетки способны замещать поврежденные или утраченные клетки и с одинаковой эффективностью функционировать в различных органах и системах организма.
Этот результат имеет большую значимость в медицине и открывает возможности для разработки новых методов лечения различных заболеваний и травм, связанных с повреждениями тканей.

0 Комментариев