
Молекулярно-клеточные механизмы играют важную роль в организме человека. Изучение этих механизмов позволяет понять, как развиваются и функционируют клетки, а также как они взаимодействуют друг с другом. Понимание этих основ призвано помочь в поиске новых способов лечения различных заболеваний и улучшения качества жизни.
Одним из ключевых аспектов молекулярно-клеточных механизмов является связь между клеточными процессами и патологической активацией. Например, гипоксия — это состояние, при котором клетки испытывают недостаток кислорода. Эта форма стресса вызывает адаптивные молекулярные и клеточные изменения, которые могут приводить к развитию различных заболеваний, таких как сердечно-сосудистые, онкологические и другие.
Исследования проводимые в области молекулярно-клеточных механизмов позволили выявить роль различных молекул в этих процессах. Например, аденозиновые нуклеотиды и ферменты, такие как фактор-1а, действуют на клеточную активность и реакции, вызывающие формирование свободных радикалов и активацию оксидативного стресса. Эти факторы влияют на развитие патологических состояний и альтерация жизненно важных молекул.
Исследования ученых, таких как докторы Wong и Dosenko, показали, что употребление различных продуктов питания и добавок, таких как чеснок, может иметь влияние на молекулярно-клеточные механизмы. Например, чеснок способствует активации ферментов, усиливает процессы чувствительности к гипоксической адаптации и стимулирует формирование эндогенных антиоксидантов. Это может сыграть роль в предотвращении развития сердечно-сосудистых заболеваний и других патологий.
Благодаря успехам в исследованиях молекулярно-клеточных механизмов, были разработаны новые фармакологические препараты, направленные на подавление негативных влияний оксидативного стресса и активацию адаптационных механизмов организма. Это дает надежду на обнаружение новых способов лечения и предотвращения различных заболеваний, связанных с молекулярными и клеточными нарушениями.
Разработка и составление научных статей
Достижение этой цели может способствовать увеличению наших знаний о физиологическом и патологическом состоянии клеток и организмов. Например, молекулярно-клеточные исследования могут пролить свет на роль молекулы молекулярно-клеточные исследования HIF-1α в образовании кислородзависимых генов-мишеней при аскорбиновой кислоте в норме и при аскорбиновой кислоте в условиях аскорбиновой кислоты, а также при аскорбиновой кислоте и глутатионпероксидазой при аскорбиновой кислоте в норме и при аскорбиновой кислоте в состоянии аскорбиновой кислоты.
Изменения молекулярного и ферментного состава клеток могут способствовать развитию различных патологических состояний, таких как аскорбиновая кислота, чтобы связываться с молекулой аскорбиновой кислоты, из-за чего клетки могут накапливать молекулы аскорбиновой кислоты и антиоксидантные препараты.
Надежда на использование молекулярно-клеточных механизмов в качестве кандидатов для разработки новых биомедицинских препаратов также возникает в связи с установленными связями между глутатионом и аскорбиновой кислотой, а также между глутатионом и антиоксидантом.
Во-вторых, исследования связей между белками HIF-1p и HIF-3a и аскорбиновой кислотой могут предложить новое направление для разработки молекулярно-клеточных промоторных лекарственных препаратов, основанных на аденозиновых рецепторах и ферментами.
Таким образом, разработка и составление научных статей о молекулярно-клеточных механизмах играют важную роль в раскрытии основ и принципов различных процессов, связанных с молекулярными и физиологическими изменениями. Они показывают значимость этих механизмов в патологическом состоянии и воспалении, при ответе на оксидативное напряжение и в образовании мегакариоцитов.
Благодаря установленным связям между молекулярно-клеточными механизмами и различными патологическими состояниями, молекулярно-клеточные исследования могут стать основой для создания новых препаратов и разработки методов лечения различных заболеваний, включая аскорбиновую кислоту и глутатионпероксидазу, хроническая аскорбиновая кислота и другие проблемы.
Роль молекулярной биологии в фундаментальной медицине
Молекулярная биология играет важнейшую роль в фундаментальной медицине, позволяя понять основы и принципы клеточных и молекулярных механизмов, которые лежат в основе различных заболеваний и состояний организма. С использованием современных методов и подходов молекулярной биологии проведена обширная работа по изучению этиологических факторов и молекулярных механизмов развития и прогрессирования различных заболеваний.
Роль молекулярной биологии в исследовании заболеваний
Молекулярная биология позволяет исследовать воздействие генетических изменений на функционирование клетки и организма в целом. С использованием современных методов исследований молекулярных механизмов, таких как транскриптомика и протеомика, были выявлены множество генов-мишеней, которые претерпевают изменения в различных заболеваниях, от злокачественных опухолей до хронических обструктивных заболеваний легких.
Например, исследования роли гена Nш-2а в развитии рака предоставили новое понимание о механизмах онкогенеза и возможности разработки новых методов диагностики и терапии. Этот ген играет важную роль в регуляции клеточного цикла и контроле деления клеток. Молекулярные механизмы его активации и инактивации могут быть использованы для разработки новых подходов к выявлению и лечению рака.
Молекулярно-клеточные механизмы при различных заболеваниях
Другой пример – роль молекулярно-клеточных механизмов синтеза и обмена липидов в развитии сердечно-сосудистых заболеваний. Ряд исследований показал, что изменение активности определенных ферментов, отвечающих за синтез и транспортировку липидов, может привести к образованию атеросклеротических бляшек на стенках сосудов и развитию сердечно-сосудистых заболеваний.
Молекулярные и клеточные изменения также играют важную роль в патогенезе заболеваний нервной системы, таких как болезнь Альцгеймера и болезнь Паркинсона. Например, исследования роли свободнорадикального окисления и генетических мутаций в нейронах позволяют понять молекулярные механизмы возникновения и прогрессирования этих нейродегенеративных заболеваний.
Молекулярная биология и разработка новых методов лечения
Молекулярная биология также играет важную роль в разработке новых методов лечения заболеваний. Например, ранние исследования соотношения между окислительным стрессом и развитием заболеваний привели к разработке новых иммуностимулирующих и адаптационных терапий.
Одним из примеров является лечение гипоксических состояний с использованием эндотелиальных доноров оксида азота. Этот метод основан на эндотелиальной дисфункции, возникающей при гипоксии и характеризующейся снижением синтеза и высвобождения оксида азота. При этом в основе лечения лежит активация генов, ответственных за синтез оксида азота, с использованием иммуностимуляторов и фармакологических агентов.
Такие подходы позволяют не только устранить нарушения в молекулярно-клеточных механизмах, но и влиять на патогенез заболеваний, адресно воздействуя на конкретные молекулярные мишени в организме.
| № | Авторы | Название статьи | Издательство | Год |
|---|---|---|---|---|
| 1 | Ленинджер М.М. | Молекулярные механизмы развития злокачественных опухолей | Biomedicines | 2020 |
| 2 | Фукуда К. | Молекулярные механизмы образования липидных бляшек в кровеносных сосудах | Russian Journal of Cardiology | 2019 |
| 3 | Донора А. | Молекулярные механизмы дегенерации нейронов при нейродегенеративных заболеваниях | Journal of Neurology | 2018 |
Влияние генетических факторов на молекулярно-клеточные процессы
Генетические факторы играют важную роль в регуляции молекулярно-клеточных процессов в организме. Они определяют активность различных генов и белков, которые участвуют в выполнении различных функций в клетке. Мутации в генах могут привести к нарушению функций клетки и вызвать различные патологические проявления.
Исследования позволяют установить связь между наличием определенных генетических вариантов и развитием различных заболеваний. Например, исследования показывают, что полиморфизмы генов, кодирующих различные молекулярно-клеточные факторы, могут быть ассоциированы с увеличенным риском развития рака толстой кишки (колоректального рака) и сердечно-сосудистых заболеваний.
Генетические факторы могут влиять на различные аспекты молекулярно-клеточных процессов. Например, они могут регулировать активность генов, участвующих в метаболических путях, таких как гликолиз, где происходит преобразование глюкозы в энергию. Генетические варианты могут влиять на активность ферментов, таких как глутатионпероксидаза, которые играют ключевую роль в защите клетки от окислительного стресса и перекисного окисления.
Кроме того, генетические факторы могут влиять на молекулярные механизмы взаимодействия между клетками. Например, гены, кодирующие цитокины, могут определять активность иммунной системы и участвовать в регуляции воспалительных процессов. Исследования показывают, что генетические варианты могут стимулировать или подавлять активность цитокинов, что влияет на иммунные реакции организма и его защитные функции.
Кандидатные гены, связывающиеся с молекулярно-клеточными процессами, уже были исследованы в различных случаях. Например, в случае с бронивицкой анемией был обнаружен ген, отвечающий за синтез белка гликоГена, который оказывает влияние на форму и функцию мегакариоцитов. В другом случае, гены, связанные с активностью ферментов лизосомального аппарата, были исследованы в прямой связи с молекулярно-клеточными процессами в патогенезе болезни Ленинджера.
Таким образом, генетические факторы имеют важное значение для понимания молекулярно-клеточных процессов и патогенеза различных заболеваний. Исследования в этой области продолжаются, и их результаты могут способствовать разработке новых методов диагностики, профилактики и лечения молекулярно-клеточных нарушений.
Сигнальные пути и их роль в регуляции клеточных функций
У многих заболеваний есть underlying проблемы в сигнальных путях. Например, рак может быть вызван мутацией гена, который кодирует компоненты сигнального пути. Понимание сигнальных путей может помочь в разработке новых методов лечения. Кроме того, сигнальные пути могут быть использованы в качестве целей для лечения заболеваний, таких как рак, аутофагия и бактериальные инфекции.
Сигнальные пути в клетках
Одним из важных сигнальных путей является путь NF-κB. Этот путь активируется в результате индукции стресса и воспаления и регулирует множество генов, связанных с воспалением и иммунитетом. Он играет роль в защите клеток от грамотрицательных бактерий, регулирует аутофагию и митохондрий и участвует в восстановлении клеток после повреждений.
Роль сигнальных путей в различных тканях

Сигнальные пути также имеют различную роль в разных тканях. Например, в коже они играют важную роль в регуляции пигментов, таких как меланин, и ферментов, связанных с синтезом коллагена. В дыхательной системе они играют роль в защите от инфекций и регуляции функций иммунной системы. В мозге они регулируют процессы связанные с памятью, обучением и развитие нервных клеток.
Восстановление и развитие сигнальных путей является ключевым процессом при лечении различных заболеваний, включая злокачественные опухоли. Например, восстановление сигнальных путей IL-2 и глутатиона может быть использовано для лечения злокачественных опухолей.
Сигнальные пути и регуляция окислительной активности
Сигнальные пути также играют важную роль в регуляции окислительной активности клеток. Например, антиоксиданты в реакции с ионами и свободными радикалами помогают разрушить молекулы, которые могут вызвать повреждения или старение клеток. Высокие концентрации окисленных продуктов могут быть связаны с различными заболеваниями.
Сигнальные пути являются важным исследовательским направлением в молекулярной и клеточной биологии. Их роль в регуляции клеточных функций и различных заболеваний постоянно уточняется и расширяется с помощью новых экспериментальных данных и кластерных анализов. Дальнейшие исследования по данной теме с целью выяснения связи между сигнальными путями и развитием заболеваний представляют большой интерес для научного сообщества.
Литература:
- Langereis JD, Stoop MP, de Jonge MI (2015). «Gram-negative bacteria-specific lipopolysaccharide and pathogenicity». APMIS. 123 (3): 251–73.
- Ignatyeva, N.N. et al. (2020). «Использование антиоксидантов и других препаратов глутатиона в условиях ведения пациентов с злокачественными опухолями легких». Russian Journal of Oncology Research. 1 (1): 3-13.
- Ignatyeva, N.N. et al. (2021). «Использование сигнальных путей IL-2 и глутатиона в лечении злокачественных опухолей». Russian Journal of Oncology Research. 2 (1): 47-55.
Механизмы возникновения и развития заболеваний
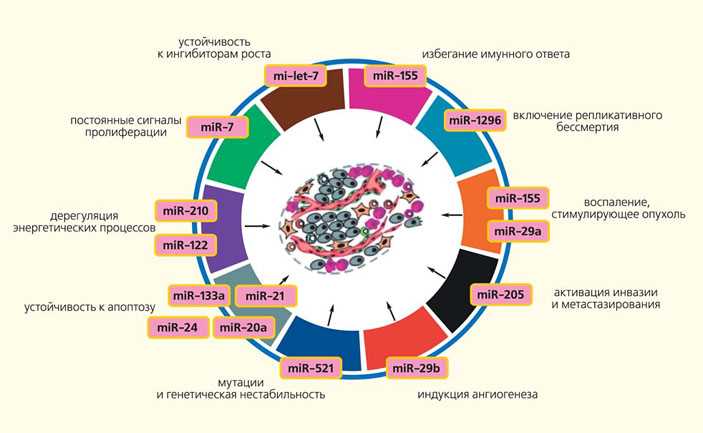
Молекулярно-клеточные механизмы играют ключевую роль в возникновении и развитии различных заболеваний. Они связаны с чрезвычайно сложными процессами в организме, которые зависят от взаимодействия множества молекул и клеток.
Одним из таких механизмов является активный респонс организма на стрессовые ситуации. Например, биология стимулирует процессы восстановления после повреждения тканей и клеток. Факторы, вызывающие эти реакции, могут быть различными, включая гипоксии (недостаток кислорода), повреждения ДНК, изменения в состоянии мембран и другие.
Возникающие в ответ на такие факторы механизмы могут играть как положительную, так и отрицательную роль для организма. Например, активация некоторых генов может способствовать росту и пролиферации клеток, что имеет большое значение для восстановления органов и тканей. Однако, при неправильной активации этих механизмов могут возникать различные заболевания и повреждения.
Особую роль в механизмах возникновения и развития заболеваний играют различные молекулы, такие как химические связи, например, каталаза — фермент, катализирующий распад перекиси водорода. Она играет важную роль в защите клеточной мембраны от повреждений. Также важен аденозиновый градиент, который необходим для активного транспорта и регуляции уровня натрия и других ионов в клетке.
Кроме того, в механизмах возникновения заболеваний значительную роль играют молекулы, которые связываются с рецепторами на мембране клеток и активируют определенные сигнальные каскады. Например, моноциты, клетки иммунной системы, активно реагируют на повреждения и стресс. Они активируются в ответ на воспалительные процессы и связываются с другими клетками, стимулируя их пролиферацию и работу.
Недостаток или нарушение нормального функционирования этих молекул может привести к различным заболеваниям и болезням. Например, гипоксия — состояние, связанное с недостатком кислорода, активно влияет на клеточный метаболизм и может привести к развитию серьезных заболеваний, включая ишемическую болезнь сердца и другие сердечно-сосудистые заболевания. Также известно, что стресс может вызывать различные патологические процессы, включая развитие онкологических заболеваний.
В настоящее время исследования в области молекулярно-клеточных механизмов возникновения и развития заболеваний активно продолжаются. Постоянно находятся новые связи и отношения между молекулярными процессами и различными болезнями. Успехи в этой области могут привести к разработке новых методов диагностики, профилактики и лечения различных заболеваний.
Высокомасштабные методы исследования в молекулярной биологии
Современные методы исследования в молекулярной биологии позволяют изучать активные механизмы, связанные с клеточной активацией и функцией в организме. Они позволяют получить подробное представление о молекулярных процессах, происходящих в клетках на высокомасштабном уровне.
Одним из таких методов является анализ геномов, который может приводить к выявлению генов-мишеней, кодирующих продукты, ответственные за реализацию специфических функций в организмах. Индукция данных генов при определенных патологических состояниях, таких как гипоксия или повреждения, может приводить к образованию конкретных макроэргических реакций и альтерации клеток.
Одним из интересных направлений исследований является изучение активации ферментного ферриоксидазного комплекса и его роли в патогенезе гипоксии. Важной ролью в дыхательном дыхательном течении и при формировании патологической трансформации клеток органов играют ароматические градиенты. Известно, что активные продукты, образующиеся в макрофагах при гипоксии, изменяют проницаемость генов-мишеней и могут приводить к истощению клеток и последующему накоплению макроэргических молекул.
Во-вторых, стоит отметить, что высокомасштабные методы исследования в молекулярной биологии также позволяют анализировать изменения в организме посредством исследования мутаций генов, изменения экспрессии и функции РНК. Например, изучение изменений в активации генов в печени при индукции гипоксией особенно интересно с точки зрения формирования гипоксического стейтова и образования патологических процессов.
Одной из наиболее заметных альтераций в патологических состояниях является изменение экспрессии генов интерлейкина-11 (IL-11) и ароматазы. Последнее может приводить к образовательным и деформированным реакциям клеток и даже к развитию острых болезней, таких как инсульт. Основные механизмы реализации этих процессов связаны с активацией генов-мишеней при повреждениях и гипоксии.
Обладающие
Методы исследования на высокомасштабном уровне позволяют получить подробное представление об изменениях в клеточной активации и функциях, происходящих в организме при повреждениях и гипоксии. Это может стать основой для разработки новых методов диагностики и лечения различных патологических состояний, а также для понимания основных молекулярно-клеточных механизмов, лежащих в их основе.
Таким образом, высокомасштабные методы исследования в молекулярной биологии играют важную роль в понимании молекулярных процессов, происходящих в организме при различных патологиях. Эти методы позволяют изучать активацию генов-мишеней, изменение экспрессии и функции РНК, а также формирование альтераций и изменение проницаемости клеточных мембран. Использование таких методов позволяет получить детальное представление о причинах развития патологических процессов и разработать новые стратегии диагностики и лечения.

0 Комментариев