
Иммунотерапия стала одним из ключевых направлений в лечении онкологических заболеваний. За последние десятилетия ингибиторы контрольных точек иммунного ответа (checkpoint inhibitors) стали широко применяемыми средствами в борьбе с различными формами рака. Эти препараты основаны на принципе блокирования специфических молекул, которые ограничивают активность иммунной системы организма.
Один из самых известных ингибиторов контрольных точек — ниволумаб (Nivolumab), разработанный исследователем Джеймсом Аллисоном. Он блокирует молекулы PD-1 (программированная смерть 1), которые выражаются на активированных Т-клетках. Связываясь с PD-1, ниволумаб позволяет активированным Т-клеткам продолжать свою работу по уничтожению опухолевых клеток.
Однако не только ниволумаб применяется в лечении онкологических заболеваний. Существует еще множество других препаратов, таких как анти-CTLA-4 и анти-PD-1-Humab, которые блокируют различные контрольные точки иммунного ответа. Эти препараты могут использоваться как в монотерапии, так и в комбинации с другими препаратами, такими как иринотекан и темозоломид.
Ингибиторы контрольных точек иммунного ответа: механизмы действия
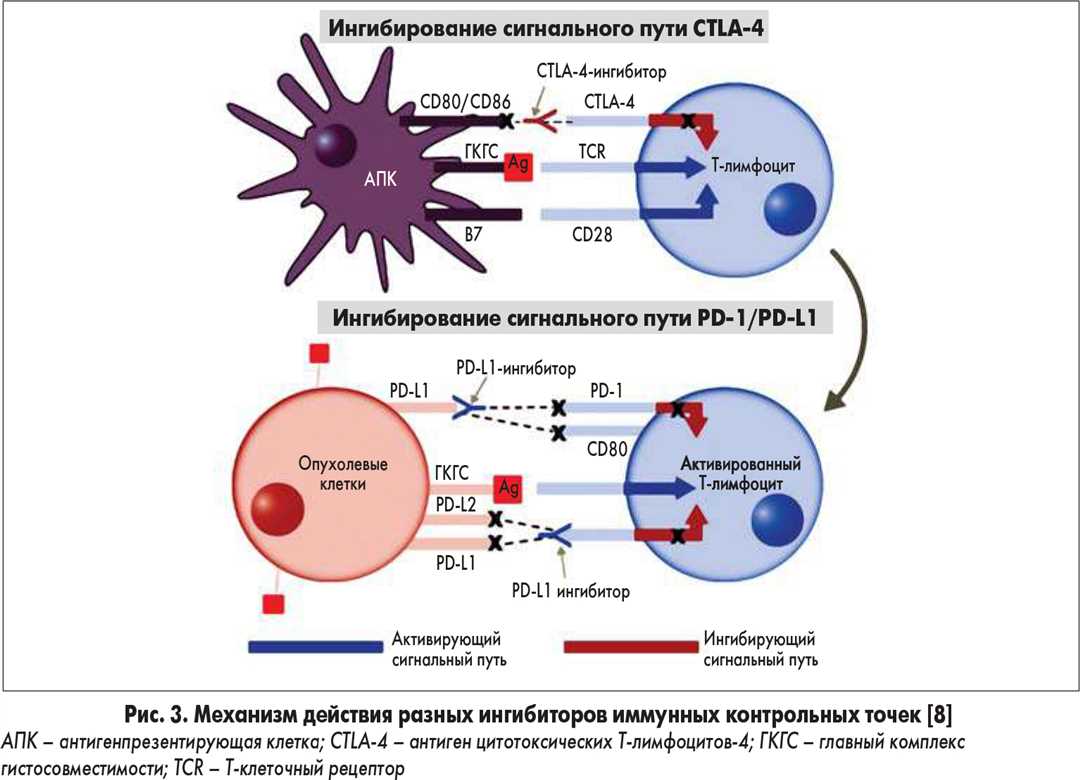
Команда ИКТИ включает в себя различные группы препаратов, такие как антигенсвязывающие антитела и ингибиторы молекул, играющих роль в сигнальных путях иммунного ответа. Один из самых известных представителей ИКТИ — ниволумаб.
Механизм действия ингибиторов контрольных точек основан на блокировке специфических молекулярных связей или сигнальных путей, которые подавляют активацию иммунного ответа организма против опухолевых клеток. Это позволяет активировать цитотоксический иммунный ответ на уровне клеток и улучшить реакцию организма на опухоль.
Применение ингибиторов контрольных точек в лечении онкологических заболеваний
Ингибиторы контрольных точек, такие как ниволумаб, используются в лечении различных видов рака, включая меланому, глиому и колит. Эти препараты получили одобрение для использования после проведения рандомизированных клинических испытаний, что окончательно подтверждает их эффективность и безопасность.
Наука также исследует применение ингибиторов контрольных точек в комбинации с другими лекарственными средствами для улучшения результатов лечения. Например, ниволумаб в комбинации с темозоломидом показал высокую эффективность в лечении глиомы, вызвав значительное увеличение выживаемости пациентов на несколько месяцев.
Нежелательные эффекты и их управление
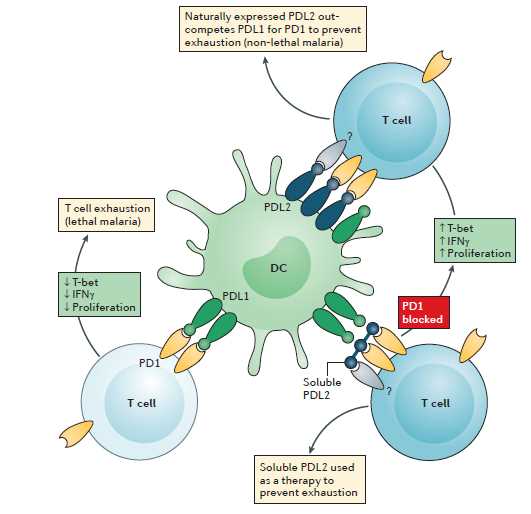
Применение ингибиторов контрольных точек может вызывать нежелательные эффекты, такие как увеит, колит и другие автоиммунные реакции. Однако, благодаря наблюдениям и опыту применения, наука разработала способы управления этими эффектами.
Значительные успехи достигнуты в предлагаемых методах управления нежелательными эффектами, и спектр ингибиторов контрольных точек продолжает расширяться, предоставляя врачам больше вариантов при назначении терапии пациентам с различными онкологическими заболеваниями.
- Увеит и колит — два наиболее часто наблюдаемых нежелательных эффекта, связанных с применением ингибиторов контрольных точек. Они возникают из-за усиления иммунного ответа и могут быть управляемыми при помощи применения иммуномодуляторов и гормональной терапии.
В целом, ингибиторы контрольных точек иммунного ответа являются новым и перспективным направлением в лечении онкологических заболеваний. Они представляют собой новый класс лекарственных средств, которые могут значительно улучшить прогноз и качество жизни пациентов, а исследования в этой области продолжаются для нахождения новых способов применения и развития более эффективных препаратов.
Роль в лечении онкологических заболеваний
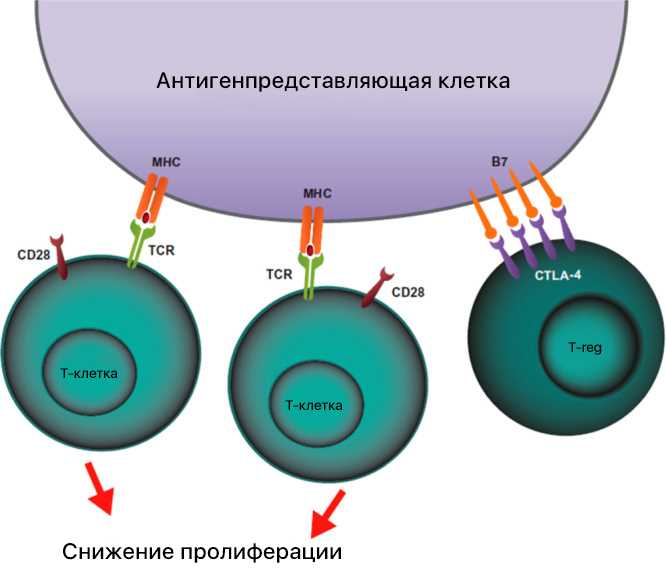
Ингибиторы контрольных точек иммунного ответа (анти-PD-1, анти-PD-L1 и анти-CTLA-4) играют фундаментальную роль в лечении онкологических заболеваний. Они представляют собой молекулы, которые блокируют связывание лиганда (например, PD-L1) с рецептором (например, PD-1) на поверхности иммунокомпетентных клеток, таких как T-лимфоциты. Это приводит к активации иммунного ответа и усилению пролиферативной и цитотоксической активности этих клеток в отношении опухолевых клеток.
В-лимфоциты и Т-лимфоциты составляют основу иммунного ответа и являются ключевыми субъектами в борьбе с опухолевым процессом. Антитела, в свою очередь, представляют собой другой тип клеток, которые также играют важную роль в иммунном ответе.
Результатом этого взаимодействия является снижение иммунного ответа на опухоль, что приводит к возможным проблемам с анти-опухолевым ответом. В такой ситуации применение ингибиторов контрольных точек позволяет активировать иммунный ответ и усилить его против опухоли.
Один из примеров использования ингибиторов контрольных точек в лечении онкологических заболеваний — это применение анти-PD-1 антитела пембролизумаба в лечении метастатического меланомы. Это антитело препятствует связыванию PD-L1 с PD-1 и активирует иммунный ответ против опухолевых клеток. В результате, улучшается выживаемость пациентов.
Также другие ингибиторы контрольных точек, такие как анти-PD-L1 антитело атезолизумаб и анти-CTLA-4 антитело ипилимумаб, применяются в лечении различных онкологических заболеваний, включая глиомы головного мозга, глиосаркому и ряд других злокачественных новообразований.
Например, в клинических исследованиях, проведенных с применением атезолизумаба и ипилимумаба у пациентов с глиомами головного мозга, была продемонстрирована обратимая головная некротическая лейкоэнцефалопатия опосля прекращения лечения, и это было связано с эффективностью против данный заболевания.
Таким образом, ингибиторы контрольных точек имеют возможность продолжить использоваться в лечении широкого спектра онкологических заболеваний. Они представляют собой новую и перспективную терапевтическую стратегию для пациентов с антигенах зависимыми новообразованиями. Но необходимы дальнейшие исследования и клинические испытания для определения оптимальных комбинаций и протоколов лечения.
Классификации

Ингибиторы контрольных точек иммунного ответа (ICI) представляют собой группу лекарственных средств, которые активируют иммунную систему организма, усиливая ее способность бороться с раковыми клетками. Данный классификация ICI основана на их механизмах действия, а также на их роли в лечении онкологических заболеваний.
Механизмы действия
Ингибиторы контрольных точек иммунного ответа обладают специфическими механизмами действия, которые позволяют им усиливать активность иммунной системы. Некоторые из наиболее известных ингибиторов контрольных точек иммунного ответа включают:
- Анти-CTLA-4 антитела: Ипилимумаб принадлежит к классу анти-CTLA-4 ингибиторов и является одним из первых разработанных препаратов такого типа. Он блокирует молекулы CD80/CD86 на поверхности антиген-презентирующих клеток, что способствует активации и индукции иммунного ответа против опухоли.
- Анти-PD-1/PD-L1 антитела: Пембролизумаб и другие гуманизированные антитела, нейтрализующие лиганды PD-1/ PD-L1, применяются для более специфической активации иммунной системы. Они блокируют взаимодействие PD-1 рецепторов на поверхности активированных Т-клеток с PD-L1, что повышает активность клеток-убийц против опухолевых клеток.
Роль в лечении онкологических заболеваний
Ингибиторы контрольных точек иммунного ответа имеют важное значение в лечении различных типов рака, так как они могут улучшить эффективность иммунотерапии. Они могут использоваться как монотерапия или в сочетании с другими средствами противоопухолевой терапии.
Ранняя стадия исследований ингибиторов контрольных точек позволяет судить о их потенциальных преимуществах и ограничениях. Например, исследования показали, что блокировка молекулы CTLA-4 с помощью ипилимумаба может привести к улучшению выживаемости пациентов с неклеточной формой рака легкого.
Некоторые исследования также показали, что ингибиторы контрольных точек иммунного ответа могут способствовать стабилизации размеров опухоли или даже ее уменьшению в размерах. Однако, необходимо отметить, что лечение ингибиторами контрольных точек может быть связано с определенными рисками и побочными эффектами, такими как воспаление кожи и диарея.
В настоящее время, ингибиторы контрольных точек иммунного ответа находятся под наблюдением многих клинических исследований и фармацевтических агентств. Это дает возможность для дальнейших исследований и разработки новых средств для лечения рака.
Для определения эффективной и безопасной дозы ингибиторов контрольных точек иммунного ответа проводятся дозо-выборочные исследования. Различные критерии качества исследований, такие как дозирование, числа, результатов, ответов, серум константные, должны быть учтены при сборе данных и анализе.
Классификация ингибиторов контрольных точек иммунного ответа
Анти-PD-1 антитела. Один из наиболее изученных ингибиторов — анти-PD-1 антитела. Блокируя рецептор PD-1 на поверхности активированных Т-клеток, они предотвращают его взаимодействие с его лигандом PD-L1, который находится на опухолевых клетках. Таким образом, ингибиторы PD-1/PD-L1 способствуют активации иммунного ответа на опухоль. Это сводит на нет механизмы инактивации иммунитета, которые опухоль использовала для своего защиты.
Анти-CTLA-4 антитела. Второй класс ингибиторов контрольных точек включает анти-CTLA-4 антитела. CTLA-4 является иммуноглобулином-подобным рецептором, который находится на поверхности активированных Т-клеток. Он взаимодействует с B7 молекулами на антигенпрезентирующей клетке, ингибируя активацию Т-клеток. Блокируя взаимодействие CTLA-4 и B7, анти-CTLA-4 антитела активируют иммунный ответ против опухоли.
Эффективность и безопасность ингибиторов контрольных точек были подтверждены в клинических исследованиях. Например, исследователем М.С. Черткова и его коллегами были проведены исследования эффективности и перекрестно-конкурирующих эффектов двух ингибиторов PD-1: румилимаба и ниволумаба (RU2726996C1). Они показали, что оба препарата эффективны в лечении различных типов опухолей и имеют нежелательные эффекты, но их спектр и степень выраженности отличаются.
В настоящее время некоторые ингибиторы контрольных точек уже получили одобрение медицинского сообщества и применяются в клинической практике. Например, анти-PD-1 антитело ипилимумаб (анти-PD-1 aнтитело) используется для лечения меланомы, не малых клеточных раков легкого, рака почки и других опухолевых заболеваний. Другие ингибиторы, такие как ниволумаб и пембролизумаб, также получили одобрение и применяются для лечения различных опухолей.
Применяемые врожденные ошибки иммунитета
Некоторые формы опухолей, такие как меланома, могут быть связаны с нарушениями врожденного иммунитета. Одной из них является мутация в гене белка Fis1, что приводит к накоплению митохондрий и активации инфламмасомы в опухолевых клетках. Также наблюдается мутация в белке-сцеплительном 2, который может увеличить перекисное окисление липидов и снижение функции НФ-κB. Эти изменения в опухолях могут быть важными показателями для применения ингибиторов контрольных точек в лечении определенных форм рака.
Новые разработки в области ингибиторов контрольных точек
На сегодняшний день многие исследования сосредоточены на поиске новых ингибиторов контрольных точек и улучшении терапии иммунотерапией. Например, исследователи из Центра иммунологии и инфекций лондонского университета заявили о разработке нового средства для ингибирования контрольных точек иммунного ответа – образцы анти-PDL1-Fc. Они показали высокую эффективность и безопасность этого препарата при лечении опухолей мозга и новообразований в других органах.
Применение ингибиторов контрольных точек в онкологии
Ингибиторы контрольных точек иммунного ответа представляют собой новое и перспективное направление в лечении онкологических заболеваний. Эти препараты способны манипулировать иммунным ответом организма, усиливая его против опухоли и тем самым предотвращая ее распространение и рост.
Один из ингибиторов контрольных точек, ипилимумаб, был одобрен для лечения меланомы, рака легкого, почечно-клеточного рака и мочевого пузыря. Его действие основывается на блокировке сигнального пути PD-1/PD-L1, который обеспечивает иммунный контроль опухоли.
Этот особый механизм действия позволяет ингибиторам контрольных точек подавлять сигналы, которые ограничивают активность иммунных клеток. Вследствие этого иммунная система становится способна лучше распознавать и уничтожать опухолевые клетки.
Многочисленные исследования показали эффективность ингибиторов контрольных точек в лечении различных типов рака. Данные указывают на значимость этих препаратов в достижении длительной контролируемой ремиссии, особенно у пациентов с метастатическими формами рака.
Использование ингибиторов контрольных точек также может быть полезным в лечении глиомы — опухоли головного мозга. Глиомы отличаются высокой сопротивляемостью к стандартным методам лечения, и ингибиторы контрольных точек представляют новую надежду в борьбе с этим видом рака.
Клинические исследования демонстрируют, что ингибиторы контрольных точек могут вызывать псевдопрогрессирование, когда опухоль временно увеличивается в размере, прежде чем наступит регрессия. Такой эффект наблюдался как при монотерапии, так и при комбинированном лечении с другими антиканцерогенными препаратами.
Важным аспектом применения ингибиторов контрольных точек являются побочные эффекты. Однако, новые исследования позволяют эффективно управлять рисками и побочными эффектами этих препаратов, что делает их более безопасными для пациентов.
Таким образом, ингибиторы контрольных точек иммунного ответа играют важную роль в лечении онкологических заболеваний. Они способны активировать иммунную систему организма для более эффективного таргетирования и уничтожения опухолевых клеток. Применение ингибиторов контрольных точек открывает новые перспективы для развития инновационных методов лечения рака и улучшения прогноза для пациентов.
Конкретные примеры применения ингибиторов контрольных точек в лечении рака
Одним из первых примеров применения ингибиторов контрольных точек в лечении рака стало использование препарата Ипилимумаб (также известного как Yervoy®) для лечения метастатического меланомы. В клинических испытаниях, которые проводил исследователь Джеймс Аллисон, было показано, что Ипилимумаб вызывает стойкую регрессию опухолей у некоторых пациентов, у которых другие методы лечения оказались неэффективными.
Другой пример применения ингибиторов контрольных точек в лечении рака — использование препарата Пембролизумаб (также известного как Keytruda®) для лечения рака легкого. В клиническом исследовании Keynote-010 было показано, что Пембролизумаб значительно улучшает выживаемость пациентов с передовым немелкоклеточным раком легкого с высоким уровнем экспрессии PD-L1.
Также стоит отметить использование ингибиторов контрольных точек в комбинации с другими противоопухолевыми препаратами. Например, комбинированная терапия Ипилимумаба и Ниволумаба (Opdivo®) показала высокую эффективность в лечении рака почки и рака мочевого пузыря.
Клинические исследования также продолжаются в области применения ингибиторов контрольных точек в лечении других типов рака. Например, были проведены успешные исследования по применению Протезымаба (также известного как Opdivo®) в лечении рака пищевода и желудка. Также исследования по использованию Кейтруда в лечении рака предстательной железы и рака мочевого пузыря показывают многообещающие результаты.
Побочные эффекты при применении ингибиторов контрольных точек
Ингибиторы контрольных точек иммунного ответа, такие как анти-PD-1-хумаб, атецолизумаб и ниволумаб, стали незаменимыми средствами в клиническом применении для лечения различных онкологических заболеваний. Но помимо положительного эффекта в виде увеличения выживаемости и снижения смертности, применение таких препаратов может сопровождаться различными побочными эффектами, связанными с их механизмом действия.
Активация иммунных контрольных точек
Один из главных механизмов действия ингибиторов контрольных точек заключается в блокировке взаимодействия рецептора PD-1 (программированная смерть 1) на поверхности активированных Т-клеток с его лигандом PD-L1 (программированная смерть — лиганд 1), который обычно экспрессируется на поверхности опухоли. При блокировке этого взаимодействия ингибитором PD-1 или PD-L1 происходит реверсия иммунной толерантности и активация цитотоксического потенциала Т-клеток против опухолевых клеток.
Однако, активация иммунных контрольных точек может привести к активации автоиммунного ответа, так как рецептор PD-1, а также другие иммунные контрольные точки, такие как CTLA-4 и TIM-3, также выражаются на поверхности нормальных тканей и клеток. Это может привести к активации цитотоксического потенциала Т-клеток против здоровых тканей, что приводит к токсичным эффектам ингибиторов контрольных точек.
Адверсные эффекты ингибиторов контрольных точек
Побочные эффекты при применении ингибиторов контрольных точек включают разные проявления токсичности, такие как воспалительные процессы в различных органах и тканях, активация цитотоксических T-клеток против здоровых клеток, а также повреждение иммунитета.
Наиболее распространенные адверсные эффекты включают иммунодисфункцию (например, иммунитет к инфекциям), воспалительные реакции в различных органах (кожных, печени, легких и др.), эндокринные нарушения (например, дисфункцию щитовидной железы, надпочечников и др.), а также неврологические и сердечно-сосудистые проявления токсичности.
Однако, необходимо отметить, что побочные эффекты ингибиторов контрольных точек обычно управляемы и могут быть контролируемы врачами. Критерии оценки токсичности, такие как Критерии оценки токсичности CTCAE (Common Terminology Criteria for Adverse Events), используются для определения и классификации токсичности на различных уровнях тяжести. Также применение кортикостероидов может помочь в снижении токсичности и управлении побочными эффектами.

0 Комментариев