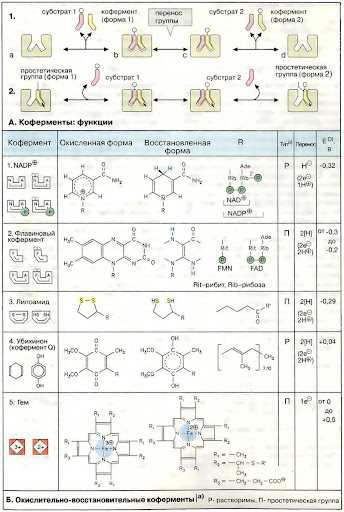
Окислительно-восстановительные реакции (ОВР) в биохимии играют важную роль в поддержании жизнедеятельности организмов. Они представляют собой процессы переноса электронов, которые межмолекулярно передаются от окислителя к восстановителю. При этом, восстановитель принимает электроны, становясь окислителем, а окислитель отдает электроны, становясь восстановителем.
В основе ОВР лежит принцип движения электронов внутри органических и неорганических молекул. Ключевую роль в этих процессах играют растворы, в которых растворены окислители и восстановители. Разность потенциалов между двумя электродами, находящимися в этих растворах, называется редокс-потенциалом. Он выражается величиной электродного потенциала и позволяет оценить энергию окислительно-восстановительной реакции. Разность потенциалов органического и неорганического электрода составляют окислительный потенциал и восстановительный потенциал соответственно.
ОВР имеют следующие особенности: 1) при участии органического вещества происходит дегидрирование, то есть отвод водорода; 2) окислитель и восстановитель связанные в единую систему образуют мембранный метаболизм; 3) растворы разной степени ионизации используют кофакторы восстановителя; 4) окислитель и восстановитель принимают участие в разных реакциях, образуя полуреакции; 5) ОВР могут быть связаны с образованием не только воды, но и различных продуктов.
Биохимические ОВР играют важную роль в организме. Они обеспечивают постоянство внутренней среды организмов, а также участвуют в обмене веществ. Например, при дыхании в клетках организма происходит окисление органических веществ с участием ОВР, что позволяет выделять энергию. Эти реакции также влияют на состав клеточных мембран и их полупроницаемость. Благодаря ОВР организмы получают энергию для своего метаболизма.
В результате проведенных исследований было установлено, что различные реакции ОВР связаны с образованием разных фрагментов и имеют различные степени свойств полуреакций. Также было установлено, что для протекания ОВР существуют определенные правила. Один из таких принципов – правило случаев, которое учитывает различные характеристики окислителя и восстановителя, такие как редокс-потенциалы элементов, их ионизации и связанные с ними реакционные ряды.
Особенности биохимических окислительно-восстановительных процессов в организмах
В основе окислительно-восстановительных реакций лежит передача электронов от одного вещества к другому. При этом, окисление означает потерю электрона, а восстановление – его приобретение. Эти процессы отражаются в изменении окислительного состояния вещества.
Цепь редокс-процессов может происходить через перенос электронов на разные уровни энергии. Для этого используются различные окислители и восстановители. Например, восстановителем может выступать аскорбиновая кислота, а окислителем – кислород.
Основная реакция окисления-восстановления в организмах связана с дыхательной цепью. В ее процессе происходит передача электронов от донора (которым является NADH) к акцептору (которым является кислород). При этом выделяется энергия, которая используется для синтеза АТФ, основной энергетической молекулы клеток.
Биохимические окислительно-восстановительные реакции обладают разной степенью окисления и восстановления. Они могут быть стандартными или нестандартными, в зависимости от значений потенциалов окислительного и восстановительного соединений.
Важной особенностью биохимических окислительно-восстановительных процессов является наличие свободных радикалов. Они обладают высокой реакционной способностью и могут вызывать повреждение клеток и тканей. Однако, организмы обладают системами антиоксидантной защиты, которые предотвращают негативное воздействие радикалов.
Биохимические окислительно-восстановительные процессы нарушаются в патологических состояниях организма. Например, в нейродегенеративных заболеваниях наблюдается нарушение метаболизма окислительно-восстановительных реакций в мозге, что приводит к повреждению нейронов и развитию патологических изменений.
Для регистрации параметров биохимических окислительно-восстановительных реакций используют различные методы, включая электрохимический метод с использованием электродных систем. Например, путем регистрации потенциала водородного электрода можно оценить окислительно-восстановительный потенциал и степень окисления-восстановления в растворах и живых системах.
Глава 8. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ И ПРОЦЕССЫ
Окислительно-восстановительные реакции и процессы в организмах играют ключевую роль в множестве жизненно важных функций. Они позволяют организмам принимать участие в метаболических процессах, связанных с использованием и переработкой кислорода.
Одним из основных видов окислительно-восстановительных реакций является дыхательная фосфорилирование, которое происходит в митохондриях клеток. В ходе этого процесса окисление органических веществ, таких как углеродные соединения, сопровождается образованием АТФ — основного энергетического компонента клетки.
Восстановление кислорода является одним из ключевых этапов дыхания и происходит благодаря активной участию ферментов, таких как цитохром оксидаза. В ходе реакции образуются вода и энергия, которые несут в себе необходимые свойства и функции для поддержания жизнедеятельности организмах.
Основные особенности окислительно-восстановительных реакций связаны с высокой скоростью их протекания в организмах. Они являются стандартным способом обмена веществ, при котором происходит передача электрона от окислителя к восстановителю.
Восстановительный процесс может происходить при образовании свободнорадикального виде, когда на электроде образуется атом вещества, обладающий высокой активностью. Существуют различные условия, при которых возможно проявление свойств окислительно-восстановительного процесса, включая давление, температуру и pH среды.
Известно, что железо является одним из ключевых ионов, участвующих в окислительно-восстановительных реакциях. Оно может принимать различные значения окислительного и восстановительного потенциала в условиях организма.
Дыхательные процессы, такие как дегидрирование, а также газовая фаза дыхания, в основе своей имеют окислительно-восстановительный характер. Они осуществляют перенос атомов водорода между различными органическими и неорганическими соединениями.
Окислительно-восстановительная связь имеет большое значение для биохимических процессов в организмах. Она позволяет совершать перенос электронов и образование различных продуктов, включая воду и углеродную кислоту.
Благодаря своим особым свойствам, окислительно-восстановительные реакции и процессы играют важную роль в многих аспектах жизнедеятельности организмов. Они являются основой для метаболических процессов и имеют большое значение в механизмах поддержания жизни.
Редокс-процессы в живых организмах
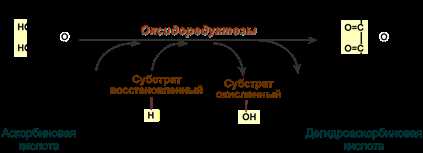
В основе редокс-процессов лежит перенос электронов от окислителя к восстановителю. Окислители – вещества, способные принять электроны, а восстановители – вещества, способные отдать электроны. Электроны передаются через цепь восстановительных и окислительных реакций, образованием которых участвуют разные виды кофакторов и доноров электронов.
Важной особенностью редокс-процессов является возможность утилизации и регистрации энергии процессами дегидрирования и окисленных форм переноса электронов. Одной из самых важных форм участия в редокс-процессах является газовая форма кислорода, которая участвует в образовании водородной связи. Молекулярный кислород является одним из переносчиков веществ в организме, в том числе исключительно важным веществом для легких в жизнедеятельности.
Самым известным правилом в редокс-процессах является правило Ленингера, которое связывает окислительно-восстановительную реакцию с переносом протона. Важной особенностью редокс-процессов является их способность каталитических реакций. Кофакторами, участвующими в редокс-процессах, являются различные молекулярные структуры, такие как флавиновые нуклеотиды, глюкоза, динуклеотиды и другие биологически активные молекулы.
Все редокс-процессы в организме следуют принципу сохранения энергии, или принципу сохранения энергии, где каждое вещество можно написать с учетом уравнения окислительно-восстановительной реакции.
Основы редокс-процессов в биохимии
Биохимические редокс-процессы играют важную роль в основах биохимии. Они являются ключевыми механизмами превращения энергии и синтеза более сложных молекул из простых органических соединений. Редокс-процессы часто сопровождаются образованием свободных радикалов, которые влияют на клеточные процессы и могут быть и сильными окислителями, и сильными восстановителями.
Окислительно-восстановительные реакции
Окислительно-восстановительные реакции являются важной группой реакций в биохимии. Они включают процессы окисления и восстановления, при которых происходит обмен электронами между реагентами. Цель таких реакций – увеличить энергетическую эффективность метаболических путей и обеспечить жизненно важные функции организма.
Наиболее известными окислительно-восстановительными реакциями являются процессы дыхания и фотосинтеза. В дыхании электроны переносятся с окислении доноров на акцепторы электронов, такие как молекулярный кислород. В результате образуется энергия, которая используется для синтеза АТФ и выполняет роль восстановителя в реакциях клеточного дыхания.
Таким образом, редокс-процессы являются основными механизмами окислительно-восстановительных реакций в живых организмах. Они играют важную роль в обмене энергии и синтезе сложных молекул, обеспечивая нормальное функционирование клеток и организма в целом.
ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА — ТОМ 2. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ — 2014
Особенности окислительно-восстановительных реакций проявляются в том, что они протекают под воздействием кислорода или других окислителей, а также восстановителей, в межмолекулярной среде. Однако, реакции окисления и восстановления также могут происходить без участия внешних окислителей или восстановителей, при этом между субстратами реакций образуются свободные радикалы.
Другим примечательным свойством окислительно-восстановительных реакций является способность атомов и ионов принимать участие как в окислительных, так и в восстановительных процессах. Окислительно-восстановительные реакции основаны на возможности атомов менять степень окисления, в результате чего происходит образование различных оксидов и веществ с разной электрохимической активностью.
Редокс-процессы имеют важное значение для жизнедеятельности организмов, так как позволяют эффективно использовать окислительно-восстановленные субстраты для получения энергии в форме АТФ (аденозинтрифосфата) и для синтеза биологически активных соединений. Скорость окислительно-восстановительных реакций может меняться в широком диапазоне и зависит от различных факторов, включая рН среды, температуру, концентрацию реагентов и др.
Окислительно-восстановительные реакции могут происходить в растворах или внутри клеточных органелл. В результате данных реакций происходит перенос электронов от одного атома к другому, что сопряжено с образованием различных продуктов реакции и изменением энергетического потенциала системы. Сумма потенциалов окисления и восстановления составляют редокс-потенциал реакции.
Окислительно-восстановительные реакции являются основой биоэнергетики и метаболизма. В процессе окисления и восстановления органических веществ, таких как сахара и жирные кислоты, осуществляется высвобождение энергии, которая используется организмами для выполнения работы и поддержания жизнедеятельности.
Таким образом, понимание основ биохимических окислительно-восстановительных реакций является ключевым для изучения биоэнергетики и метаболизма организмов, а также позволяет объяснить многие особенности и принципы энергетического обмена в биологических системах.
| 8. | Редокс-процессы | образуют | основу | окислительно-восстановительных | реакций | |||
| Скорость | окислительно-восстановительных | реакций | может | меняться | величиной | |||
| Организмы | используют | окислительно-восстановительные | реакции | для | утилизации | продуктов | ||
| Окислительно-восстановительные | реакции | позволяют | организмам | получать | энергию | для | своей | жизнедеятельности |
Виды биохимических окислительно-восстановительных процессов
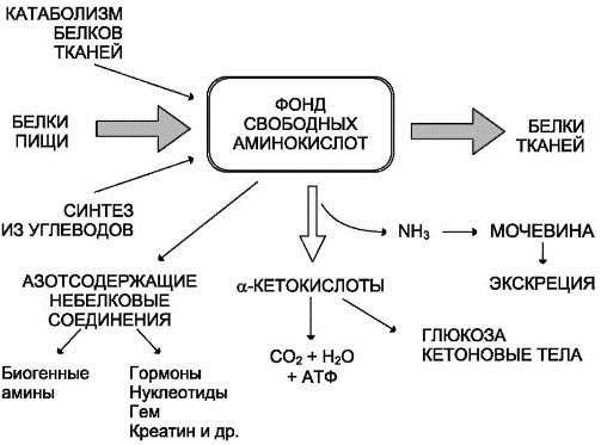
Восстановительная способность вещества определяется его потенциалом или склонностью принять электроны и/или протоны и перейти в окисленное состояние. В случаях, когда электроны или протоны переносятся между молекулами, процесс называется переносом электронов или протонов.
В основе ОВ-процессов лежит механизм, известный как окисление-восстановление. Во время окисления вещество теряет электроны и/или протоны, а во время восстановления электроны и/или протоны передаются этому веществу. Процессы окисления и восстановления обратимы и могут происходить под разными условиями.
Для описания ОВ-процессов используется понятие потенциала водородного ионизации (pH), который является мерой концентрации водородных ионов в растворе. При нейтральном pH значение равно 7, а при более низком pH есть кислота, а при более высоком — щелочь.
В мембранных органеллах, таких как митохондрии, существуют разные формы ОВ-реакций, в которых различные ферменты участвуют в окислительно-восстановительных процессах. Особенности митохондриальных ОВ-процессов связаны с тем, что электроны и протоны переносятся через митохондриальные мембраны, что позволяет создать протонный градиент для синтеза АТФ.
Видно, что восстановленные и окисленные формы атома или группы атомов могут существовать в рамках одного вещества, образуя так называемую пару окислительно-восстановительных форм. Потеря электронов и/или протонов основной окисленной формой объясняется уравнением полуреакции.
Общепринятые классификации ОВ-процессов основаны на различных качественных и количественных характеристиках. Один из подходов — классификация процессов по виду переноса электронов от одного вещества к другому. Виды ОВ-процессов включают перенос электронов между молекулами (включая транспорт электронов в дыхательной цепи), перенос электронов между разными атомами в рамках одной молекулы (как, например, в ферментативных реакциях), перенос водорода между молекулами и другие виды ОВ-процессов.
Таким образом, разнообразие биохимических окислительно-восстановительных процессов связано с различными механизмами и особенностями переноса электронов и протонов в организме. Эти процессы играют важную роль во многих важных биохимических реакциях, таких как дыхание, синтез АТФ и другие обменные процессы.

0 Комментариев