Эритроциты – красные кровяные клетки, выполняющие важную функцию по переносу кислорода от легких к тканям организма. Они содержат гемоглобин – белок, способный связываться с кислородом и удерживать его внутри клетки. Таким образом, наличие нормального количества и функционирование гемоглобина крайне важно для поддержания нормального обмена веществ в организме.
Одним из наследственных дефектов генов, кодирующих различные компоненты гемоглобина, является генетический дефект ферментов, ответственных за метаболические процессы в эритроцитах. Нарушение работы этих ферментов приводит к гемолитическим анемиям – заболеваниям, связанным с повышением разрушения эритроцитов и снижением количества гемоглобина. Одним из наиболее известных генетических дефектов является эритроцитарная глюкозо-6-фосфатдегидрогеназная дефицитность (Г6ФДД).
Г6ФДД – наследственное заболевание, нарушающее работу фермента глюкозо-6-фосфатдегидрогеназы, который участвует в процессе обмена веществ в эритроцитах. При его дефиците возникает недостаток фермента, что приводит к нарушению работы цикла переноса энергии и связанного с ним процесса образования энергии в клетках эритроцитов. Это ведет к повышению уровня окисленных продуктов, таких как перекись водорода, внутри клетки. Повышенный окислительный стресс может привести к повреждению мембраны эритроцитов и их преждевременному разрушению – гемолизу. При этом появляется классическая клиническая картина гемолитической анемии с желтушностью кожи и склер.
Недостаток глюкозо-6-фосфатдегидрогеназы Г-6-ФД в эритроцитах
Недостаток Г-6-ФД относится к классу наследственных ферментных дефицитов и является наследуемым в автомоссомном рецессивном или доминантном режиме. У пациентов с недостатком Г-6-ФД наблюдается нарушение энергетических процессов в эритроцитах, что приводит к обусловленным гемолизинами кризам и клинической гемолитической анемии.
Возникновение недостатка Г-6-ФД связано с нарушением работы генов, кодирующих белки, ответственные за функции фермента. Этот генетический дефект ведет к недостаточности активности Г-6-ФД и нарушению энергетического обмена в эритроцитах. Таким образом, эритроциты становятся более уязвимыми к внешним факторам, что приводит к их повреждению, гемолизу и возникновению клинических симптомов.
Клинические проявления недостатка Г-6-ФД могут включать гемолитическую анемию, ретикулоцитоз, анемию предшественников, морфологическое изменение эритроцитов и видимых обломков эритроцитов. Недостаток Г-6-ФД также может быть источником развития других заболеваний, включая онкогематологические нарушения.
Недостаток Г-6-ФД может быть обнаружен в любом возрасте, но чаще проявляется в детском или молодом возрасте. Он может быть установлен с помощью лабораторных методов, измеряющих активность фермента Г-6-ФД в эритроцитах. У пациентов с недостатком Г-6-ФД рекомендуется избегать определенных лекарственных препаратов и факторов, которые могут вызвать гемолитическую кризу.
Лечение недостатка Г-6-ФД может включать поддерживающую терапию, направленную на снижение клинических проявлений гемолитических кризов, а также на предотвращение их возникновения. При обнаружении недостатка Г-6-ФД необходимо обратиться к специалисту, так как он может быть связан с различными патологиями, включая поражение внутренних органов, в том числе мозга.
Ферментный дефект и его последствия
Ферментный дефект в эритроцитах может иметь разные формы и проявляться по-разному у разных людей. Некоторые формы имеют более тяжелое течение, характеризующееся частыми кризовыми состояниями и анемическими признаками. В других случаях, дефект может проявиться в менее выраженной форме, с более мягкими симптомами.
Одним из наиболее известных ферментных дефектов в эритроцитах является овалоклеточная анемия, обусловленная дефектом гена, который кодирует фермент, связывающий два предшественника в процессе синтеза шариковидной формы эритроцитов. Это заболевание характеризуется изменением формы эритроцитов, что приводит к ухудшению их функций и возможным развитием гемолитической анемии.
Ферментный генетический дефект в эритроцитах может вызвать различные последствия для организма. В результате сниженной активности или отсутствия ферментов происходит нарушение обмена веществ, что может привести к различным негативным последствиям, таким как гемолитическая анемия, образование камней в почках, спленомегалия, нарушение функции печени и другие.
Гемолитическая анемия
Одним из наиболее распространенных и серьезных последствий ферментного генетического дефекта в эритроцитах является гемолитическая анемия. В случаях, когда ферментный дефект вызывает повышенную разрушаемость эритроцитов, происходит ускоренный гемолиз эритроцитов, что приводит к снижению их числа и развитию анемии.
Спленомегалия
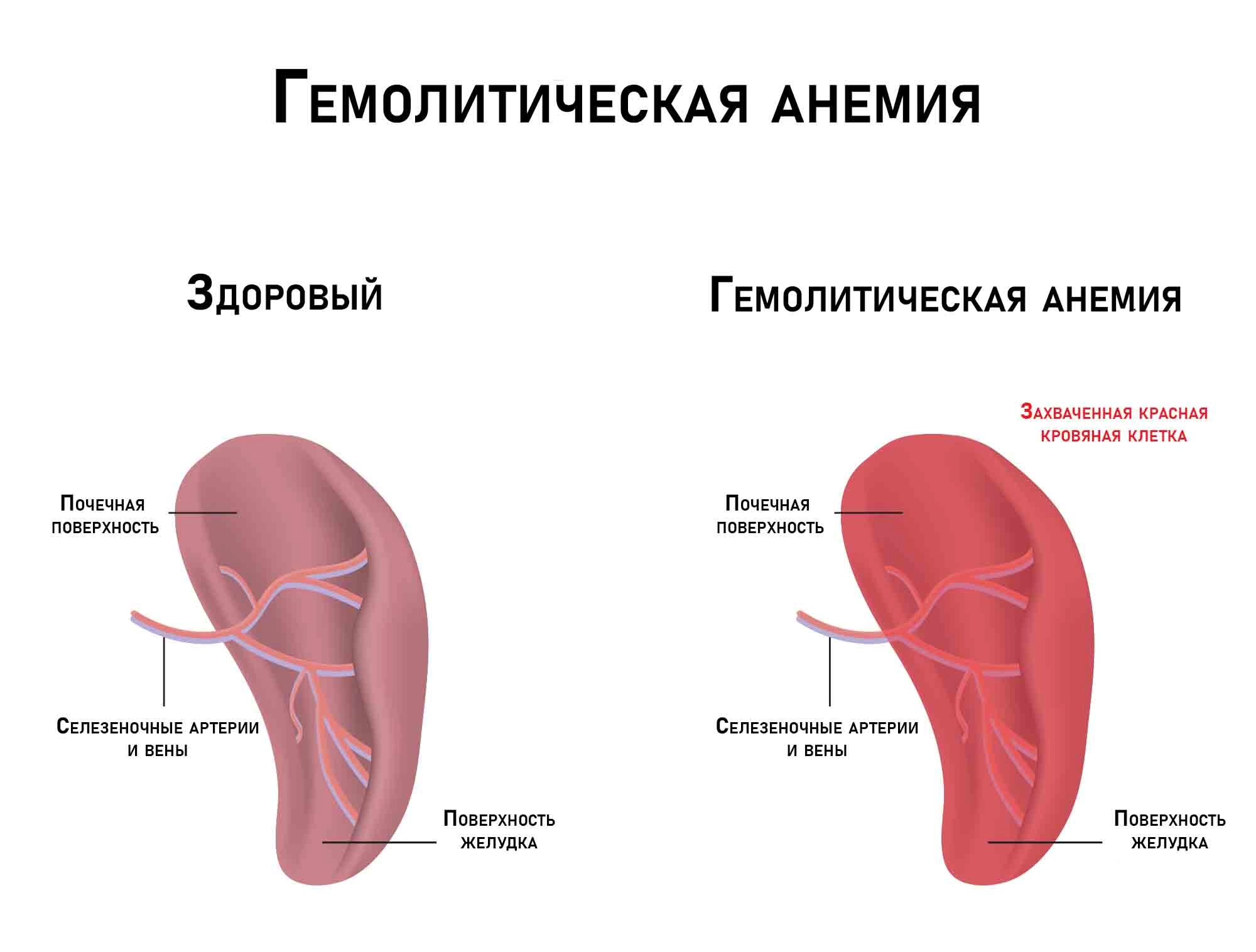
Спленомегалия, или увеличение размеров селезенки, также может быть одним из последствий ферментного дефекта в эритроцитах. Увеличение селезенки обычно связано с увеличенной разрушаемостью эритроцитов, что приводит к усиленной работе селезенки с целью удалить поврежденные эритроциты из кровотока.
Нарушение функции печени
Ферментный генетический дефект в эритроцитах также может повлиять на функцию печени. В ряде случаев, ферментный дефект может вызывать нарушение обмена веществ в печени, что может привести к развитию печеночной недостаточности.
В целом, ферментные генетические дефекты в эритроцитах могут иметь разные последствия для организма. Точное влияние и возможные осложнения зависят от конкретного дефекта и его тяжести. Отсутствие или недостаточная активность ферментов в эритроцитах может привести к различным нарушениям в обмене веществ и функционировании органов, что требует эффективной диагностики и лечения для предотвращения серьезных осложнений.
Влияние недостатка Г-6-ФД на эритроциты

Г-6-ФД ответственен за процесс образования НАДФН, который является необходимым для защиты эритроцитов от окислительного стресса. Отсутствие или недостаточность этого фермента приводит к снижению активности гексозмонофосфатного шунта, что приводит к увеличению содержания свободных радикалов и повреждению эритроцитов.
В результате, эритроциты становятся более уязвимыми, что может привести к различным нарушениям, связанным с их функциональностью и выживаемостью. У пациентов с недостатком Г-6-ФД часто наблюдается анизоцитоз, гемолизинами, холестериновые обломки эритроцитов и спленомегалия.
Недостаток Г-6-ФД является источником многих генетических заболеваний, таких как энзимопатии, особенно наследственная неспецифическая гемолитическая анемия и гемолитическая секрезиуринная анемия. Часто эти заболевания развиваются в детском возрасте, происходит спонтанная регрессия или периодически возникают кризы.
Значительное количество гемолитических напряжений вызывает активацию спленного пула у таких пациентов. Для лечения этого состояния может потребоваться спленэктомия, чтобы предотвратить развитие гемолитических кризов и обеспечить нормальную активность эритроцитов.
Таким образом, недостаток Г-6-ФД оказывает значительное влияние на эритроциты и может быть обусловлен различными генетическими мутациями. В медицине это заболевание считается одной из наиболее частых форм наследственной гемолитической анемии. Для точного определения диагноза и лечения важно проводить курсы генетического консультирования и обследования пациентов с возможными ферментными дефицитами и связанными с ними анемиями.
Диагностика генетического дефекта
Для проведения данного анализа пациенту берут кровь с помощью специальности иглы и рукавицы на фоне приема противогемолитических курсов и анемической терапии. Полученные образцы крови помещают в специальные пробирки и добавляют реактивы, позволяющие измерить активность Г-6-ФД. Результаты анализа сравниваются с нормой, чтобы определить наличие дефекта в гене, ответственном за этот фермент.
Симптомы и последствия генетического дефекта
Гемолитическая энзимопатия, обусловленная дефицитом Г-6-ФД, приводит к развитию гемолитической анемии. Этот генетический дефект характеризуется сниженной активностью Г-6-ФД в эритроцитах, что приводит к их быстрому разрушению и появлению ретикулоцитоза.
Снижение активности Г-6-ФД может проявиться уже в детском возрасте, а иногда и во время беременности. У пациентов с г-6-фд дефицитом наследственный эффект может преобладать в эритроцитах в течение жизни. Развитие гемолитической анемии на фоне Г-6-ФД дефицита может приводить к развитию билирубинемии и аномалией в составе эритроцитов.
Генетическое тестирование и консультация
Для определения генетического дефекта, отвечающего за недостаточность активности Г-6-ФД, может проводиться генетическое тестирование. Этот метод позволяет найти мутации в генах, зависимых от белковозависимых гемолитических анемий.
Консультация генетика позволяет оценить риск передачи генетического дефекта от родителей к потомству, а также обсудить возможные методы профилактики и лечения для пациента.
Методы выявления недостатка Г-6-ФД
Необходимо отметить, что генетический дефект Г-6-ФД является наиболее распространенным гемолитическим анемией, особенно в российской популяции. При этом влияние недостатка Г-6-ФД на организм является многосторонним. Одной из основных проблем, с которыми сталкиваются пациенты с недостатком Г-6-ФД, является гемолиз (разрушение красных кровяных клеток). Гемолиз провоцирует развитие гемолитического криза, сопровождающегося снижением гемостаза и развитием анемии.
Для диагностики недостатка Г-6-ФД используются различные методы. Один из них — определение активности фермента Г-6-ФД в эритроцитах пациента. Этот метод широко используется в клинической медицине и является наиболее точным для выявления генетического дефекта Г-6-ФД. Кроме того, проводятся исследования генетического материала пациента на наличие изменений в генах, кодирующих Г-6-ФД. Это позволяет обнаружить наследственные аномалии связанные с Г-6-ФД. Также в ходе диагностики могут быть использованы методы изучения морфологии эритроцитов пациента, такие как анизоцитоз (измененная форма эритроцитов), овалоцитоз-1 (нарушение формы эритроцитов в виде овала или неправильной фигуры) и гиперплазия черепа (увеличение размера черепа).
Лечение недостатка Г-6-ФД довольно сложно и включает в себя ряд методов. Некоторым пациентам могут быть назначены лекарственные препараты, направленные на усиление активности ферментов и улучшение обмена веществ в эритроцитах. В некоторых случаях может потребоваться спленэктомия (удаление селезенки) для снижения гемолиза. Важно отметить, что в ряде клинических случаев лечение недостатка Г-6-ФД сводится к поддержанию нормального состояния пациента и предотвращению кризового развития анемии.
Таким образом, методы выявления недостатка Г-6-ФД в медицине являются важными инструментами при диагностике этого наследственного генетического дефекта. Они помогают определить точный генез недостатка Г-6-ФД и разработать индивидуальный план лечения для каждого пациента с учетом его особенностей и возраста.
Медицинское вмешательство
В случае нарушения активности этого фермента, возникают серьезные проблемы в процессе синтеза гемоглобина, который содержится в эритроцитах и несет кислород по всему организму. Автором этой статьи, студентом Романенко, была проанализирована большая часть литературы на тему генетических дефектов и их влияния на развитие заболеваний с учетом особенностей эритроцитов, составляющих около 1/3 объема крови.
Генетические дефекты, связанные с недостатком ферментов, могут привести к различным формам гемолитической анемии, включая гемолитическую кризу, анемический период и тяжелые симптомы общего нарушения состава эритроцитов.
Одной из форм заболевания, связанных с недостатком глюкозо-6-фосфатдегидрогеназы, является болезнь Жильбера. Это наследственное заболевание, характеризующееся усилением синтеза билирубина и его недостаточным выведением из организма, что приводит к повышению его содержания в крови. Студентом Романенко была подробно рассмотрена эта форма болезни и ее проявления.
Важно также отметить, что при наличии генетических дефектов может возникать гемолитическая анемия в разных формах, с огромным числом возможных симптомов и различного уровня тяжести. В случае с генетическими дефектами, связанными с эритроцитами, особенно важна роль селезенки, которая выполняет функцию уничтожения поврежденных эритроцитов.
Лечение таких заболеваний проводится с учетом особенностей эритроцитов и генетических дефектов. Оно направлено на устранение недостатка фермента и предупреждение кризового периода. Для этого могут использоваться различные методы, включая прием препаратов, которые способствуют увеличению активности нужного фермента или подавление его дефекта.
Таким образом, медицинское вмешательство в случае ферментного генетического дефекта в эритроцитах является необходимым для улучшения качества жизни пациента и предотвращения осложнений, связанных с нарушениями состава эритроцитов и функционирования организма в целом.
Основные методы лечения недостатка Г-6-ФД
Одним из основных методов лечения недостатка Г-6-ФД является предотвращение периодов гемолиза. Пациенты с этим генетическим дефектом должны избегать факторов, которые могут спровоцировать гемолитическую реакцию, таких как определенные лекарственные препараты, инфекции и питательные недостатки. При появлении клинических симптомов гемолиза, пациентам рекомендуется обращаться за медицинской помощью.
В случаях значительного нарушения синтеза Г-6-ФД, можно использовать специфические лекарственные препараты, которые способны увеличить количество этого фермента в эритроцитах и уменьшить риск гемолиза. Одним из таких препаратов является лекарственное средство N-ацетилцистеин.
Кроме того, при появлении симптомов гемолиза, врачи могут применять терапию кровообращения, включающую трансфузию эритроцитов. Эта процедура позволяет компенсировать недостаток эритроцитов и уменьшить риск развития анемии.
Важным критерием успешной диагностики и лечения недостатка Г-6-ФД является раннее обращение за медицинской помощью и прохождение специальных лекций по генетическим нарушениям. Ранняя диагностика и эффективное лечение позволяют предотвращать развитие осложнений и улучшить качество жизни пациентов с этим генетическим дефектом.
Профилактика и поддержание здоровья
Профилактика и поддержание здоровья играют важную роль в управлении ферментным генетическим дефектом в эритроцитах. В данной статье рассматривается прямая связь между генетическим дефектом, кодирующим недостаточность энзимов, таких как глюкозофосфатизомераза (Г-6-ФДГ) и эритроцитарная гликолитическая энзимопатия, с развитием различных гемолитических заболеваний.
Одним из основных методов профилактики является ранняя и точная диагностика этих генетических дефектов. Недостаточность Г-6-ФДГ и других гликолитических ферментов может привести к появлению эритроцитной дефицита и развитию гемолитических заболеваний. Точный и своевременный диагноз позволяет начать лечение раньше и предотвратить развитие клинических проявлений.
Пациентам с генетическим дефектом в эритроцитах рекомендуется следовать специальному рациону, включающему питание, богатое питательными веществами, такими как витамины и минералы. Регулярные физические упражнения и умеренная физическая активность также являются важными компонентами профилактики и поддержания здоровья.
Проведение регулярных медицинских обследований для контроля состояния эритроцитов и уровня эндогенного эритропоэтина (гормона, регулирующего образование эритроцитов) также рекомендуется для предотвращения развития возможных осложнений.
В случае гемолитических заболеваний, связанных с генетическим дефектом в эритроцитах, большая польза может быть получена от переливания донорской крови. Периодические трансфузии красных кровяных клеток могут помочь компенсировать уровень крови и снизить риск развития осложнений в связи с дефицитом эритроцитов.
Таким образом, профилактика и поддержание здоровья играют ключевую роль в управлении ферментным генетическим дефектом в эритроцитах. Ранняя диагностика, правильное питание, регулярные физические упражнения и контроль медицинского состояния являются важными составляющими для предотвращения развития клинических проявлений и поддержания здоровья пациента.

0 Комментариев