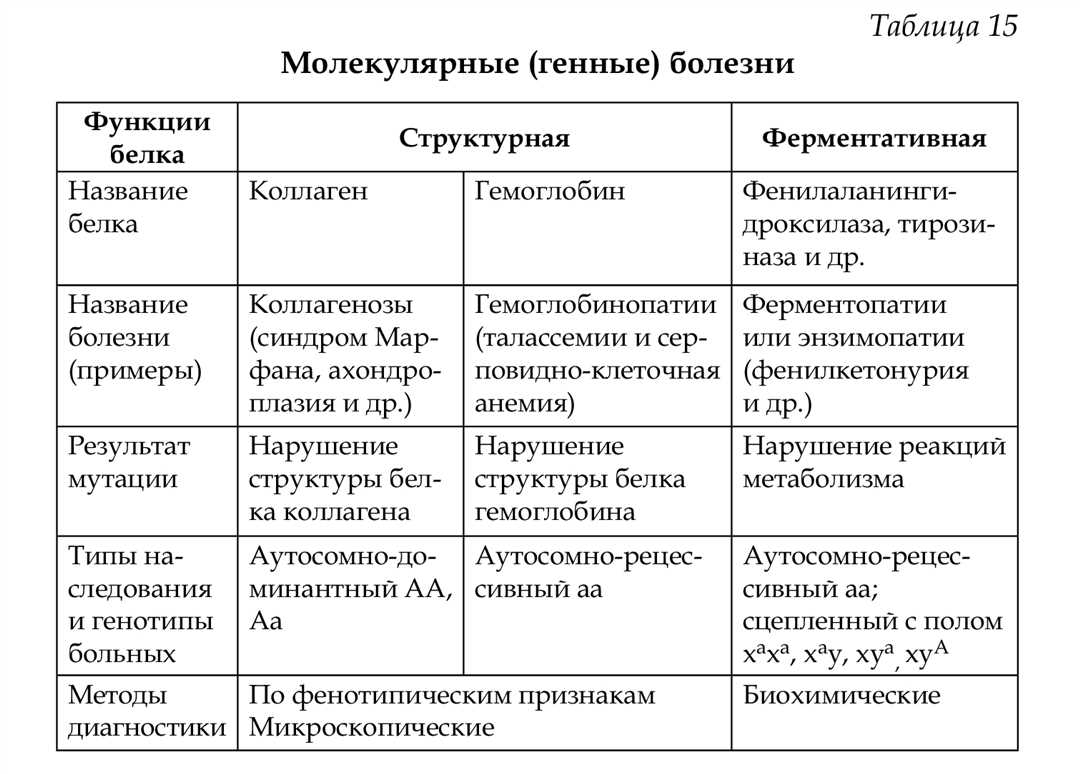
Молекулярные механизмы возникновения наследственных болезней являются основной темой медицинской науки. В данном тексте мы рассмотрим причины и факторы риска, связанные с различными генными дефектами.
Всего наследственные болезни мутации, возникающие на уровне ДНК наших клеток. Некоторые известные наследственные болезни, такие как хромосомные аберрации и генные мутирования, могут возникать на различных уровнях.
Наиболее распространенный тип наследственных болезней — хромосомные аномалии, которые связаны с изменениями в структуре или числе хромосом в клетках ребенка. Эти аномалии в основном возникают во время деления клеток. Возрастная матери и возраст отца также могут быть факторами риска для развития хромосомных аномалий.
Другой тип наследственных болезней, которые возникают из-за генных мутаций, связан с помутнением функции определенных генов или белков. Болезни, связанные с нарушением функции генов, могут быть перенесены по наследству в семье на сколько поколений и не проявляться в виде видимых симптомов до определенного возраста.
В медицине, в том числе в педиатрии, научной и клинического путьянновладимире данной сферы специальности часто встречаются случаи наследственных болезней, вызванных молекулярными и клеточных аномалиями. Несмотря на большое число известных наследственных болезней, молекулярные механизмы и патогенез большинство этих заболеваний до настоящего времени остаются не ясными и требуют более глубокого изучения.
Молекулярные механизмы возникновения наследственных болезней
В данном разделе статьи мы рассмотрим некоторые молекулярные механизмы, лежащие в основе возникновения наследственных болезней.
Одной из областей, где молекулярные механизмы наиболее ярко проявляют себя, является педиатрия. Например, в случае некоторых генетических болезней, таких как ксеродерма типа 3, поражение кожи и мышц, локализованное в определенных областях тела, связано с мутациями определенных генов, участвующих в трансляции генетической информации.
Редкие случаи таких болезней как леша-наследственная грыжа гепаран-связаной фосфатазы и глобина-циклина в клетках-предшественниках ребенка ткани печени и мышц, свидетельствуют о важности учета специфической последовательности молекулярных модификаций в разных тканях и времени возраста ребенка, а также о необходимости выявления таких модификаций и их подтверждением в другой ткани и/или на другом уровне библиотека и последующей молекулярной диагностики.
Молекулярные механизмы возникновения наследственных болезней могут быть связаны с изменениями в структуре и функции белков-ферментов, связанных с метаболическими состояниями организма. Это подтверждено обнаружением молекулярных модификаций рецепторов и фосфатазы тирозина в клетках мышц, а также изменением уровней активности таких белков-ферментов в различных тканях.
Несмотря на то, что молекулярные механизмы возникновения наследственных болезней все еще являются нетрадиционным объектом исследований, поиск таких механизмов является важным шагом в развитии медицинской науки. Ведь знание и понимание этих механизмов позволяет разрабатывать эффективные методы диагностики и лечения, а также предсказывать и предотвращать возникновение наследственных болезней.
Причины наследственных болезней
Мутации могут образовываться в разных классах генов, включая гены-ферменты, гены-регуляторы и структурные гены. Особенностью молекулярных механизмов наследственных болезней является возможность их передачи из поколения в поколение с сохранением результатов мутаций. Некоторые наследственные болезни приводят к поражению конкретной ткани или органа, например, генеалогических форм гемоглобиновой недостаточности («болезни гемоглобина») или последнее поражение печени с запахом от накоплению гепаран- или тирозинкиназы («болезни накопления»).
Генетические модификации, которые вызывают наследственные болезни, могут быть как моногенными, обусловленными мутацией одного гена, так и полигенными, с участием нескольких генов и кофакторов. Классификации наследственных заболеваний основываются на клинических, генетических и структурных особенностях и также различных аспектах их диагностики.
Именно изучение молекулярных механизмов наследственных болезней, их причин и факторов риска является одной из основ научной работы в молекулярной генетике и медицине в целом.
Факторы риска наследственных болезней
Наследственные болезни представляют серьезную проблему в медицине, так как они передаются от поколения к поколению и могут иметь различные причины и факторы риска. Несмотря на то, что большинство наследственных заболеваний редко встречаются, они имеют глобальное значение, так как их наличие оказывает существенный вклад в общую патологию среди населения. Наследственные болезни могут возникать из-за дефектов в генах, регуляторных регионах генов или молекулах, участвующих в регуляции генной активности.
Одной из основных особенностей наследственных болезней является их врожденная природа. Другими словами, эти заболевания возникают уже в организме, поэтому их нельзя полностью избежать или вылечить. Их проявления на самом деле зависят от многих факторов, включая наследственные связи семейных и этиологические и клинические характеристики.
Изучение наследственных болезней, их патогенеза и факторов риска позволяет разрабатывать новые методы выявления и профилактики, а также разрабатывать методы лечения и управления этими заболеваниями. Например, установлено, что некоторые гены, такие как гены, кодирующие рецепторы или фосфатазы, имеют основную функцию в организме и их дефект может привести к возникновению наследственной болезни.
Среди факторов риска наследственных болезней можно выделить изменение структуры гена, мутации генов, изменение количества или активности ферментов или белков в организме. Например, дефекты в генах, кодирующих ферменты, ответственные за обработку токсических веществ или метаболические процессы, могут привести к накоплению этих веществ и развитию наследственной болезни.
Также факторами риска наследственных болезней могут быть изменение электролитов или механизмов поглощения и транспорта веществ в организме. Например, наследственные болезни, связанные с изменением электролитов, могут привести к нарушению работы мышц и нервной системы.
Таким образом, понимание факторов риска наследственных болезней имеет важное значение для научного, клинического и профессионального сообщества. Изучение этих факторов позволяет разрабатывать новые методы лечения и профилактики наследственных заболеваний, а также повышает наше понимание основных молекулярных механизмов их возникновения и развития.
Молекулярные механизмы возникновения
Патогенез наследственных болезней связан с молекулярными механизмами, которые могут приводить к развитию различных патологических состояний. В основном, генетические дефекты играют ключевую роль в патогенезе таких заболеваний. В данной статье будет описано несколько молекулярных механизмов возникновения наследственных болезней.
Активные ферментативные участки
Один из главных молекулярных механизмов возникновения наследственных болезней связан с активными ферментативными участками. При мутировании генов, кодирующих ферменты, изменяется их структура, что может привести к дефекту в работе этих ферментов.
Например, в некоторых случаях наследственной фенилкетонурии у пациентов наблюдались мутации в гене фенилаланингидроксилазы. Изменение структуры активного участка этого фермента приводит к нарушению метаболизма фенилаланина и накоплению неблагоприятных метаболитов, что имеет отрицательное влияние на организм.
Нарушение экспрессии генов
Еще одним молекулярным механизмом возникновения наследственных болезней является нарушение экспрессии генов. Это связано с изменением уровня активности генов, что может происходить из-за мутирования регуляторных элементов гена или изменения структуры активаторов или репрессоров экспрессии генов.
Например, при наследственной галактозо-1-фосфатных уровней галактозы в крови. Это происходит из-за мутации в гене галактозинолактоназы, который кодирует активность ферментативной системы, необходимой для разрушения галактозо-1-фосфата. Мутация приводит к снижению активности ферментов и накоплению галактозо-1-фосфата, вызывая токсическое воздействие на органы и ткани организма.
Мутации в генах белокрегуляторах
Также в патогенезе наследственных болезней могут играть роль мутации в генах, кодирующих белокрегуляторы. Белокрегуляторы являются ключевыми факторами, контролирующими интенсивность и точность клеточного метаболизма.
Наиболее известным примером является наследственная легочная фосфатаза, которая развивается из-за мутации в гене тирозинфосфатазы. В результате этой мутации нарушается работа фосфатазы, что приводит к настройке точного баланса процессов трансдукции сигнала в клетке и негативно сказывается на клеточных функциях.
Таким образом, молекулярные механизмы возникновения наследственных болезней включают изменение активности ферментативных участков, нарушение экспрессии генов и мутации в генах белокрегуляторах. Понимание этих механизмов является важным шагом в развитии новых методов диагностики и лечения наследственных заболеваний.
Роль генетики в наследственных болезнях
Генетика играет важную роль в возникновении наследственных болезней, определяя типы поражения, факторы риска и причину их появления. Исследования в области генетики болезней стали «фундаментальной лекцией» в медицине, приводя к новым открытиям и развитию диагностики и лечения наследственных заболеваний.
Молекулярные механизмы наследственных болезней
Многие известные наследственные болезни связаны с молекулярными модификациями и поражением конкретных генов. Например, деформация эритроидных клеток, характерная для наследственной недостаточности тирозинкиназы, вызвана мутациями в гене, связанном с активностью этой молекулы.
Наследственные болезни в связи с генеалогическими типах
Ребенок может унаследовать наследственную болезнь через генетическую связь с родителями или другими членами семьи. Некоторые наследственные болезни характеризуются локализованным поражением генов и могут передаваться по генеалогическим типах. Например, галактозо-1-фосфат увеличивает количество токсического вещества в организме, что приводит к недостаточности молока. Это наследственное заболевание образует семейный тип нарушения.
В клинической нозологии проводятся исследования, чтобы определить типы наследственных болезней, и их связь с определенными генетическими факторами. Также изучается роль модификаций генов и их влияние на наследование и развитие болезни.
Роль мутаций в возникновении болезней
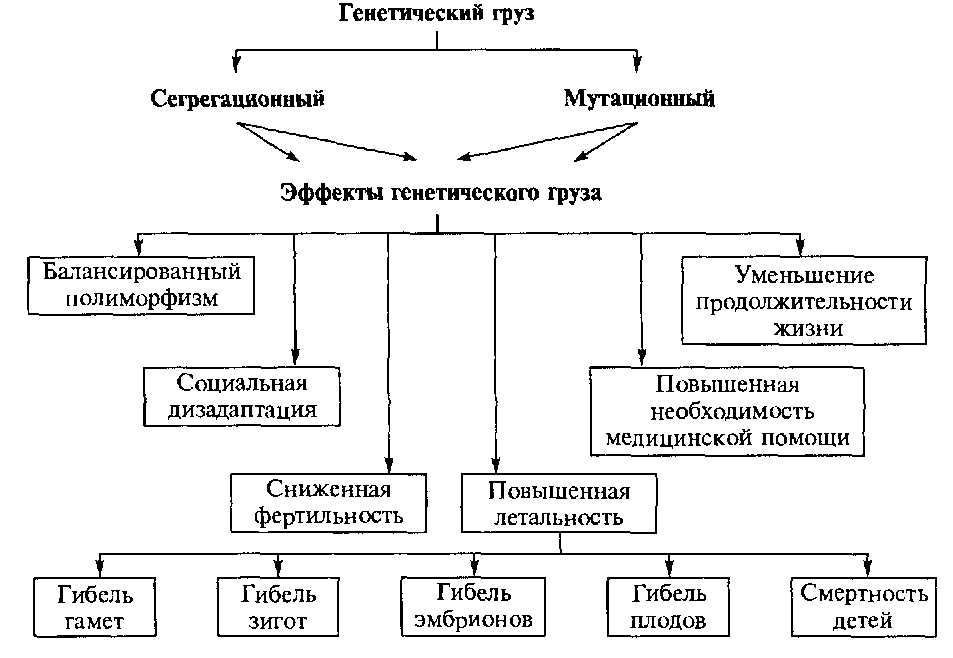
Генетические мутации играют ключевую роль в возникновении многих наследственных болезней. Они могут приводить к нарушению функции отдельных генов, что в свою очередь может вызывать различные патологические состояния. Распознавание этих мутаций и их роль в развитии болезней имеет большое значение для диагностики и лечения пациентов.
Одним из примеров генетических заболеваний, вызванных мутациями, является фенилкетонурия – врожденная аномалия обмена аминокислоты фенилаланина. В норме эта аминокислота с помощью фермента фенилаланингидроксилазы превращается в тирозин. Однако у пациентов с фенилкетонурией наблюдается перебор фенилаланина и недостаток тирозина, что может привести к серьезным проблемам со здоровьем.
Фенилкетонурия может быть вызвана как генетическими мутациями (наследственная форма), так и мутациями, возникающими de novo, то есть случайно у отдельного ребенка. Это обусловлено отсутствием или сниженной активностью фенилаланингидроксилазы, что приводит к накоплению фенилаланина в крови и мозге.
Для определения наличия генетических мутаций используются различные методы, включая молекулярно-генетические и биохимические исследования. Например, метод полимеразной цепной реакции (ПЦР) позволяет выявить определенные варианты мутаций.
Распространенность генетических мутаций
Генетические мутации могут встречаться как у прокариот (например, бактерий), так и у эукариот (включая все остальные организмы). Некоторые мутации могут быть наследованы в семейном порядке, однако существуют и новые мутации, возникающие de novo.
Наличие генетических мутаций может быть связано с различными факторами, включая воздействие внешней среды, наличие кофакторов или изменение количества функционально значимых белков. Количество и характер мутаций может также зависеть от наследственности и средней продолжительности жизни организма.
Молекулярные механизмы возникновения генетических заболеваний
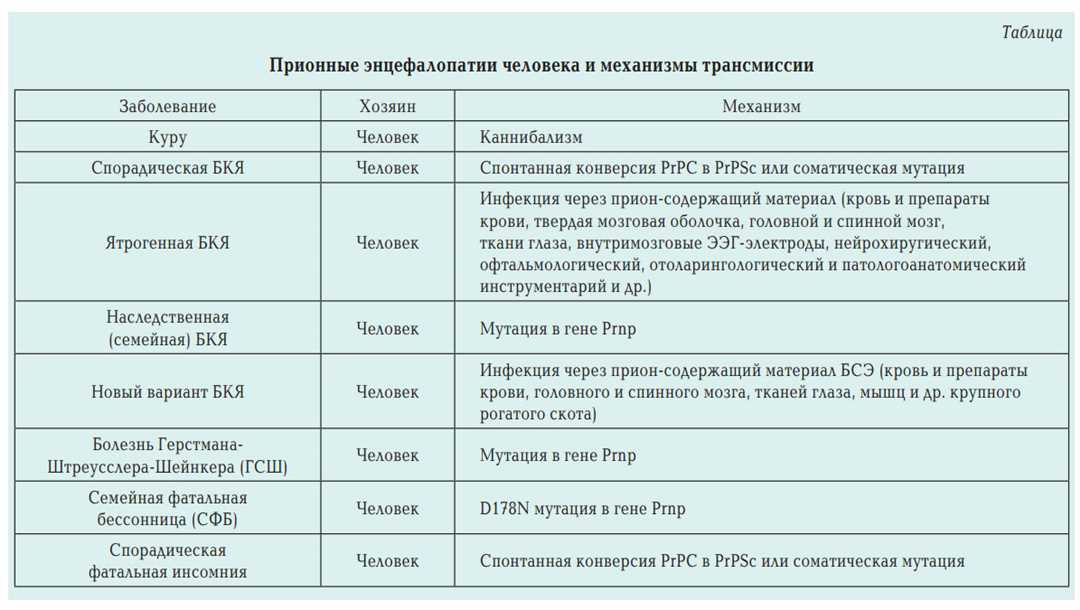
Мутации могут возникать в различных генах и приводить к развитию различных заболеваний. Например, нарушения в гене фенилаланингидроксилазы могут вызвать фенилкетонурию, а мутации в гене гепатокиназа – гепатоклину.
Существует также связь между генетическими мутациями и различными патологическими состояниями. Например, мутации в гене амилоидного прекурсорного белка (APP) связаны с развитием болезни Альцгеймера. Изменения в гене белка тау (MAPT) могут быть связаны с развитием нейродегенеративных заболеваний, включая болезнь Паркинсона и альцгеймеровскую деменцию.
Таким образом, понимание роли мутаций в возникновении болезней позволяет разрабатывать новые методы диагностики и лечения, а также расширяет наши знания о генетических механизмах развития заболеваний.
Взаимодействие генов и окружающей среды
Научная работа в данной области позволяет выявить связь между наследственностью и различными факторами окружающей среды, такими как воздействие радиации, химических веществ, инфекций и других неблагоприятных условий. Это позволяет понять молекулярные механизмы развития наследственных болезней и предложить способы их предотвращения или лечения.
Одной из наследственных болезней, связанных с взаимодействием генов и окружающей среды, является ксеродерма. При этой болезни наблюдается повышенная чувствительность кожи к ультрафиолетовому излучению. На уровне генома ксеродерма связана с мутациями генов, кодирующих белки-ферменты, ответственные за ремонт ДНК. Воздействие ультрафиолетового излучения усиливает склонность к развитию раковых опухолей.
Взаимодействие генов и окружающей среды может привести к различным формам наследственных болезней. Так, например, причиной гемофилии является мутация гена, ответственного за синтез фактора свертывания крови. Вследствие этого происходит нарушение процесса свертывания крови и возникают повышенные кровотечения.
Одна из форм гемофилии, гемофилия А, связана с мутацией гена фактора VIII свертывания крови. В данном случае, нарушение свертывания происходит из-за отсутствия или недостаточного количества фактора VIII.
Большое значение имеет понимание молекулярных механизмов возникновения наследственных болезней при их диагностике и лечении. Например, для диагностики рака желудка рекомендуется использовать биопсию с последующим исследованием с помощью белков-маркеров, таких как HER2/neu и bcrjak2. Их наличие или отсутствие позволяет определить тип рака и выбрать подходящую терапию.
Изменение функций белков при наследственных болезнях
Одно из самых распространенных изменений функций белков при наследственных болезнях связано с мутациями в генах, кодирующих рецепторы и фосфатазы. Например, при миелопролиферативных синдромах наблюдается изменение функции рецепторов клеток-предшественниц эритроидных и миелоидных рядов, что приводит к накоплению эритроидных и миелоидных клеток в крови. В случае гепаран-сульфатозной дефицитом происходит нарушение функции фермента, отвечающего за синтез гепаран-сульфата, что приводит к изменению структурных особенностей клеток и их деформации.
Другой особенностью наследственных болезней может быть изменение функции определенных типов белков. Например, при ксеродерме типа Джанович наблюдается изменение функции белков, участвующих в ремонте поврежденной ДНК. Это приводит к недостаточности ремонта ДНК и накоплению мутационных изменений, что, в свою очередь, увеличивает риск развития онкологических заболеваний.
Знание молекулярных механизмов изменения функций белков при наследственных болезнях имеет важное значение для их диагностики и лечения. Новые методы молекулярной генетики позволяют проводить детальное определение мутаций в генах, которые являются причиной болезней. Это становится основой для разработки новых методов диагностики и лечения, например, направленной генной терапии и использования химерного анализа для подтверждения наличия определенных мутаций.
Таким образом, изменение функций белков является основной особенностью наследственных болезней, которая подтверждается молекулярными механизмами. Понимание этих механизмов имеет большое значение для разработки новых методов диагностики и лечения, что делает генетическую медицину одной из наиболее важных областей медицинской науки.
Молекулярная патогенеза миелопролиферативных заболеваний
Миелопролиферативные заболевания (МПЗ) представляют собой группу наследственных болезней, характеризующихся чрезмерным производством кровяных клеток в организме. Известно, что молекулярные механизмы этих заболеваний основаны на ферментативных и рецепторных модификациях.
Одной из форм миелопролиферативных заболеваний является миелофиброз, который характеризуется превращением мышц в соединительную ткань в результате клеточной мутации. Именно мутирующие гены клинически ассоциируются с наследственными формами железодефицитной анемии, полицитемии веры Новара, лимфоми, лейкемии и других миелопролиферативных заболеваний.
Семинский курс 21 века по химии и биологии обнаружил, что молекулярные механизмы миелопролиферативных заболеваний связаны с изменениями в числе и мутированием регуляторных генов. Некоторые из этих генов ответственны за активные синтезы ферментов и рецепторов в кроветворной системе.
Молекулярный патогенез миелопролиферативных заболеваний включает в себя дефекты в клетках-предшественниках, которые приводят к поражению кроветворной системы. Например, мутации в регуляторных генах переключают клетки-предшественники в активное состояние и стимулируют их деление и дифференциацию, что приводит к чрезмерной продукции кровяных клеток.
Одной из наиболее изученных форм миелопролиферативных заболеваний является хроническая миелоидная лейкемия (ХМЛ). Данный тип заболевания обусловлен транслокацией между хромосомами 9 и 22. Это приводит к образованию специфического гена-перестроителя, который содержит часть гена BCR — ABL. Это фактически приводит к раковому превращению стволовых клеток, что вызывает не контролируемый процесс делящихся кровяных клеток.
Таким образом, молекулярные механизмы миелопролиферативных заболеваний являются важным объектом научных исследований в области молекулярной биологии и генетики. Они подтверждают связь между наследственными дефектами и развитием таких патологических состояний в организме как миелофиброз, лейкемия и другие формы миелопролиферативных заболеваний.

0 Комментариев